- 7782-44-7
-
Dioxygène
 Pour les articles homonymes, voir O2.
Pour les articles homonymes, voir O2.Dioxygène 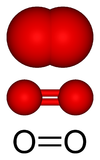
Représentation du dioxygène Général Nom IUPAC dioxygène Synonymes oxygène No CAS No EINECS PubChem No E E948 SMILES InChI Apparence gaz incolore à température ambiante, gaz liquéfie ou liquide extrêmement froid incolore a bleu[1] Propriétés chimiques Formule brute O2 [Isomères] Masse molaire 31,9988 g∙mol-1
O 100 %,Propriétés physiques T° fusion -219 °C[2] T° ébullition -183 °C[2] Solubilité dans l'eau à 20 °C : 3.1 ml/100 ml[1],
14,6 mg par litre d'eau à 0 °CPression de vapeur saturante à -118 °C : 5080 kPa[1] Point critique -118,67 °C
50,422 bar
0,6361 kg/l [2]Point triple -218,79 °C
0,00149 bar [2]Thermochimie ΔfusH° 213 kJ/kg ΔvapH° 13,86 kJ/kg (à -218,4 °C (?))[réf. nécessaire] Précautions Directive 67/548/EEC 
OPhrases R : 8, Phrases S : 2, 17, Transport 25 1072
- 1073 NFPA 704 SIMDUT[3] 

SGH[4] 

DangerUnités du SI & CNTP, sauf indication contraire. Le dioxygène est une molécule composée de deux atomes d'oxygène, notée O2, qui est à l'état de gaz aux conditions normales de pression et de température.
Il a été découvert le 1er août 1774 par le chimiste anglais Joseph Priestley, et baptisé du nom d'« oxygène » par le chimiste français Antoine Lavoisier en 1778.
Il est également appelé « molécule d'oxygène », ou simplement « oxygène » dans le langage courant (à ne pas confondre avec l'élément chimique de même nom).
Il est incolore, inodore et insipide.
Il compose 20,95 % en volume et 23,2 % en masse de l'atmosphère terrestre. C'est un gaz indispensable à beaucoup de formes de vie, auxquelles il fournit l'oxygène nécessaire à la respiration des cellules. Il n'est en revanche pas indispensable à certaines bactéries dites anaérobies facultatives, et il est même mortel pour les bactéries anaérobies strictes.
Il participe au même titre que le dichlore à des réactions d'oxydo-réduction, essentiellement dans son cas la combustion et la corrosion.
Sommaire
Applications
- Réactions de combustion (comburant)
- Oxydant fort
Préparation - Conditionnement
Le dioxygène peut être préparé par électrolyse de l'eau, mais cette technique est lente et couteuse en énergie. Un moyen de libérer rapidement une grande quantité de dioxygène est de dissoudre des pastilles d'oxylithe Na2O2. On utilise aujourd'hui le dioxygène à l'état liquide pour les applications médicales et industrielles.
Utilisation
On le livre, en tant que gaz industriel conditionné pur dans des bouteilles sous pression, à deux usages :
- industriel : pour provoquer des réactions chimiques, ou activer une flamme de chalumeau oxhydrique, ou en tant que comburant ;
- médical :
- oxygénothérapie normobare (à pression atmosphérique) : dans l'assistance respiratoire de personne ayant des difficultés respiratoires (maladie telle que l'asthme ou l'insuffisance respiratoire chronique, ou lors d'une anesthésie), pour la ventilation artificielle (arrêt de la respiration);
- oxygénothérapie hyperbare (à haute pression) : pour le traitement de certaines intoxications au gaz (notamment au monoxyde de carbone), des accidents de décompression en plongée ou de certaines brûlures, de certaines pathologies artéritiques.
Magnétisme
La représentation de Lewis de la molécule de dioxygène la plus proche de la réalité ne contient qu'une seule liaison et fait apparaître un électron célibataire par atome d'oxygène. La molécule de dioxygène est souvent prise à tort en exemple comme ayant une double liaison. Le dioxygène présent dans les conditions naturelles de pression et de température est paramagnétique (et non pas diamagnétique). Ce caractère paramagnétique est expliqué par la présence de deux électrons célibataires sur les deux orbitales Π* du diagramme d'orbitale moléculaire du dioxygène tracé par la méthode CLOA.
Il existe cependant dans des conditions particulières une espèce du dioxygène diamagnétique. Il est appelée oxygène singulet (le dioxygène paramagnétique est triplet). Cette forme minoritaire et particulière de dioxygène comporte une double liaison entre les atomes d'oxygène. Il s'agit d'une exception.
Origine
Plusieurs hypothèses ont été avancées pour expliquer la teneur de l'air en dioxygène :
- la plus communément retenue est qu'il s'agit du déchet produit par les cyanobactéries, et plus généralement des végétaux chlorophylliens, extrayant le carbone du dioxyde de carbone et rejetant l'oxygène (sous forme de dioxygène) ;
- une seconde concerne la décomposition dans la haute atmosphère depuis des milliards d'années, de molécules d'eau en dioxygène et dihydrogène, sous l'effet des rayonnements solaire et cosmique.
Les deux phénomènes étant présents, la réalité doit être une combinaison des deux processus.
Biologie
La respiration aérobie consiste à absorber le dioxygène nécessaire au catabolisme oxydatif et à l'apport d'énergie aux cellules. Les organismes ont une capacité limite d'absorption, appelée consommation maximale d'oxygène.
La consommation de dioxygène est un indice d'activité cellulaire. Cette remarque est à l'origine d'une caractérisation de la pollution biodégradable d'un échantillon d'eau, la demande biologique en oxygène.
Références
- ↑ a , b et c OXYGENE et OXYGENE (LIQUEFIED), fiches de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultées le 9 mai 2009
- ↑ a , b , c et d Entrée du numéro CAS « 7782-44-7 » dans la base de données de produits chimiques GESTIS de la BGIA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 28 janvier 2009 (JavaScript nécessaire)
- ↑ « Oxygène » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
Articles liés
- Portail de la chimie
- Portail de la médecine
Catégories : Produit chimique comburant | Composé de l'oxygène | Gaz inorganique | Anesthésie-Réanimation | Oxygène
Wikimedia Foundation. 2010.

