- 19794-93-5
-
Trazodone
Trazodone 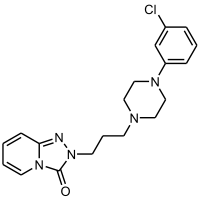
Général No CAS No EINECS Code ATC N06 SMILES InChI Propriétés chimiques Formule brute C19H22ClN5O [Isomères] Masse molaire 371,864 g∙mol-1
C 61,37 %, H 5,96 %, Cl 9,53 %, N 18,83 %, O 4,3 %,Propriétés physiques T° fusion 87 °C Unités du SI & CNTP, sauf indication contraire. Le Trazodone (Desyrel®, Trittico®, Thombran®, Trialodine®) est un composé psychoactif sédatif, anxiolytique et antidépresseur. Le fabricant affirme que l'activité d'antidépresseur devient évidente dès la première semaine de la thérapie. Trazodone à moins d'effets secondaires anticholinergiques (bouche sèche, constipation, tachycardie ) et adrenolytiques (hypotension, problèmes sexuels masculins) que la plupart des antidépresseurs tricyciques. L'incidence de la nausée et du vomissement observés avec Trazodone est relativement basse comparée aux ISRS.
Sommaire
Mécanisme d'action
Le trazodone est un inhibiteur des recapteurs de sérotonine et un antagoniste du récepteur 5-HT 2. Cependant, contrairement aux inhibiteurs sélectifs des recapteurs de sérotonine tels que le fluoxetine (Prozac®), les effets antidépresseurs des trazodones peuvent être dus à son effet antagonique à l'emplacement du récepteur 5-HT 2 (PMID 1365657).
Pharmacocinétique
Trazodone est bien absorbé après administration par voie orale, avec les niveaux maximaux moyens de sang obtenus environ 1 heure après ingestion. L'absorption est légèrement retardée et augmentée par la nourriture. La demi-vie moyenne d'élimination de sang est biphasée : la première phase de la demi vie est de 3-6 heures, et la phase suivante de 5-9 heures. Le médicament est intensivement métabolisé : 3 ou 4 métabolites principaux ont été identifiés chez l'homme, dont certains tels que mCPP peuvent contribuer au profil d'effet secondaire du trazodone. Approximativement 70-75% de C14- le trazodone marqué s'est avéré être excrété dans l'urine dans un délai de 72 heures (PMID 1037253). Trazodone est fortement lié aux protéines.
Quelques indications
- Dépression clinique avec ou sans anxiété
- Insomnie chronique (dans quelques pays, l'utilisation est multiple)
- Fibromyalgie, pour contrôler le sommeil.
- Pour le contrôle des cauchemars ou de tout autre perturbation du sommeil.
Contre-indications
- Hypersensibilité connue au trazodone
- Utilisation sur des patients en-dessous de 18 ans
Précautions
Trazodone est métabolisé par la CYP3A4, une enzyme du foie (PMID 9616194). L'inhibition de cette enzyme par d'autres substances peut retarder sa dégradation, menant à un niveau élevé de trazodone dans le sang. CYP3A4 peut être inhibé par beaucoup d'autres médicaments, herbes, et nourritures, et la trazodone peuvent donc interagir avec ces substances. Le jus de pamplemousse est notamment déconseillé pour les patients utilisant le trazodone. Un verre de jus de pamplemousse de temps à autre n'est pas susceptible d'avoir d'effet sur la plupart des personnes, mais la consommation de grandes quantité, ou le fait d'en boire régulièrement est reconnu comme causant des effets indésirables.
La possibilité de suicide pour les patients dépressifs demeure pendant le traitement et jusqu'à ce qu'un rétablissement significatif se produise. Par conséquent, les patients avec des idées suicidaires ne devraient jamais avoir accès à de grandes quantités de trazodone.
Des épisodes de convulsions partielles complexes ont été rapportés chez un nombre restreint de patients. La majorité de ces patients recevaient déjà une thérapie par anticonvulsant pour un désordre précédemment diagnostiqué de convulsion ou d'épilepsie.
Bien que le trazodone ne soit pas un vrai membre de la classe de SSRI des antidépresseur, il partage beaucoup de propriétés du SSRIs, particulièrement la possibilité de syndrome de dépendance si le médicament est arrêté trop rapidement. Il faut donc prendre soin d'effectuer un sevrage progressif en diminuant la dose sur une certaine période de temps.
Grossesse et allaitement
- Grossesse : Les données sont insuffisantes chez l'humain. L'utilisation devrait être justifiée par la sévérité de la condition à traiter.
- Allaitement : Les données sont également insuffisantes chez l'humain. Le trazodone peut être trouvé dans le lait maternel dans des concentrations significatives. L'utilisation durant l'allaitement devrait donc être soigneusement analysée en raison des risques possibles.
Effets secondaires
Les réactions défavorables les plus communes sont la somnolence, la nausée/vomissement, le mal de tête et la bouche sèche. Les réactions défavorables rapportées incluent ce qui suit :
comportemental Somnolence, fatigue, léthargie, retardement psychomoteur, distraction, vertige, difficulté dans la concentration, confusion.
neurologique Le tremblement, mal de tête, ataxie, akathisie, rigidité des muscles, le discours confus, le discours ralenti, le vertige, l'acouphène, le tintement des extrémités, la paresthesie, la faiblesse, les convulsions partielles complexes, et, le discours rarement altéré, le muscle contractant, l'engourdissement, la dystonie et les mouvements involontaires.
autonome Bouche sèche, vision brouillée, priapisme, diplopie, miosis, congestion nasale, constipation, transpiration, conservation urinaire, fréquence urinaire accrue et incontinence.
cardiovasculaire L'hypotension orthostatique, hypertension, tachycardie, les palpitations, brièveté de souffle, apné, syncope, arythmies, a prolongé l'intervalle de P.R., la fibrillation atriale, la bradycardie, l'activité ectopique ventriculaire (tachycardie ventriculaire y compris), l'infarctus du myocarde et l'arrêt cardiaque.
Effets secondaires rares
Les études cliniques récentes de patients présentant une maladie cardiaque préexistante indiquent que le trazodone peut être arrhythmogénique chez certains d'entre eux. Les arythmies identifiées incluent PVC d'isolement, couplets ventriculaires, et dans 2 battements des épisodes de patients sous peu (3 à 4) de la tachycardie ventriculaire. Il y a également eu plusieurs rapports de poteau-marketing des arythmies dans les patients trazodone-traités qui ont la maladie cardiaque préexistante et dans quelques patients qui n'ont pas eu la maladie cardiaque préexistante. Jusqu'à ce que les résultats des études éventuelles soient disponibles, des patients présentant la maladie cardiaque préexistante devraient être étroitement surveillés, en particulier pour des arythmies cardiaques. Trazodone n'est pas recommandé pour l'usage pendant la phase initiale de rétablissement de l'infarctus du myocarde.
gastro-intestinal Nausée, vomissant, diarrhée, malaise gastro-intestinal, anorexie, appétit accru.
foie On a observé des cas rares d'hépatotoxicié idiosyncratique, probablement en raison de la formation des métabolites réactifs (PMID 15978881).
Perturbateur endocrinien Diminution et, plus rarement, augmentation de libido, gain et perte de poids, et rarement, irrégularités menstruelles, éjaculation rétrograde et inhibition d'éjaculation.
On a observé des concentrations élevées de prolactine chez les patients prenant du trazodone (PMID 7673654).
Le trazodone a été associé à l'occurrence de priapisme. Dans approximativement 33% des cas rapportées, l'intervention chirurgicale a été nécessaire et a eu comme conséquence dans une partie de ces cas, l'affaiblissement permanent de la fonction érectile ou l'impuissance. Les patients masculins présentant des érections prolongées ou inadéquates doivent immédiatement cesser le traitement et consulter leur médecin. Si la condition persiste pendant plus de 24 heures, il est recommandé de consulter un urologiste ou un spécialiste approprié afin de décider d'une approche de gestion.
allergique ou toxique Éruption de peau, démangeaisons, œdème, et, rarement, anémie hémolytique, methémoglobinémie, changements d'enzymes de foie, ictère obstructif, vasculite leucocytoclastique, éruptions maculopapulaires purpuric, photosensibilité et fièvre.
Divers Joints et muscles faisant mal, yeux particuliers de goût ,de hypersalivation, douleurs de poitrine, hématurie, de rouge, fatigué et irritants.
risques professionnels Puisque le trazodone peut altérer les capacités mentales et/ou physiques exigées pour l'exécution de tâches potentiellement dangereuses, comme la conduite d'une automobile ou l'utilisation de machines, les patients doivent être avertis de ne pas s'engager dans de telles activités sous l'effet du médicament.
essais en laboratoire On lui recommande que la cellule de sang blanche et les comptes différentiels devraient être exécutés dans les patients qui développent la gorge endolorie, fièvre, ou d'autres signes de l'infection ou la dyscrasie et le trazodone de sang devrait être discontinué si la cellule de sang blanche ou le compte absolu de neutrophile tombe au-dessous de la normale.
interactions médicamenteuses Le trazodone peut augmenter les effets de l'alcool, des barbiturates et d'autres dépresseurs du SNC ; les patients devraient être avertis en conséquence.
On a rapporté que des niveaux accrus de digoxyne et de phenytoin de sérum se produisent dans les patients recevant le trazodone en même temps que l'un ou l'autre de ces 2 médicaments. Peu est connu au sujet de l'interaction entre le trazodone et les anesthésiques généraux ; donc, avant la chirurgie élective, le trazodone devrait être discontinué pour aussi longtemps que médicalement faisable.
Puisqu'on ne le connaît pas si une interaction se produira entre le trazodone et les inhibiteurs de MAO, l'administration du trazodone devrait être lancée très avec précaution avec l'augmentation progressive du dosage comme exigé, si un inhibiteur de MAO est donné simultanément ou a été discontinué peu avant le médicament avec le trazodone est institué.
Trazodone peut causer l'hypotension comprenant l'hypotension et la syncope orthostatiques ; l'attention est exigée si elle est donnée aux patients recevant des drogues d'antihypertensif et un ajustement dans la dose du médicament d'antihypertensif peut être exigé.
En raison de l'absence de l'expérience, l'administration concourante de la thérapie électroconvulsive devrait être évitée.
Dosage
Le traitement devrait être commencé par de basses doses initiales de 25 à 50 mg quotidiennement dans les doses divisées ou dans une dose simple de soirée. La dose peut être grimpée lentement à un maximum de 300 mg quotidiennement dans les patients ambulatoires et jusqu'à 600 mg quotidiennement dans les patients hospitalisés. Les patients gériatriques et émaciés devraient commencer par 100 mg quotidiennement ; cette dose peut être lentement grimpée jusqu'à 300 mg. La durée du traitement devrait être au moins d'un mois. Une dose de 50 mg est recommandée en utilisant Trazadone comme aide de sommeil.
Surdosage
symptômes Le surdosage du trazodone peut causer une augmentation d'incidence ou la sévérité de n'importe laquelle des réactions défavorables rapportées, par exemple hypotension et sédation excessive. La mort par surdosage délibéré ou accidentel a été rapportée (PMID 15975258, PMID 11603256).
traitement Il n'y a aucun antidote spécifique pour le trazodone. La gestion du surdosage devrait, donc, être symptomatique et de support. N'importe quel patient suspecté d'avoir pris un surdosage devrait être admis aussitôt que possible à l'hôpital et à l'estomac vidé par le lavage gastrique. La diurèse obligatoire peut être utile en facilitant l'élimination de la drogue.
Voir aussi
- antidépresseur
- nefazodone
Références
SID 172043 -- Sommaire De Substance De PubChem. Recherché 17 novembre, 2005. L'information de drogue de Rxlist.com. Recherché 16 janvier, 2006. L'information de drogue de Mentalhealth.com. Recherché 16 janvier, 2006.
- Traduit de en:Trazodone
- Portail de la médecine
- Portail de la pharmacie
- Portail de la chimie
Catégories : Sédatif | Antidépresseur | Chlorobenzène | Pipérazine | Azine | Triazole
Wikimedia Foundation. 2010.
