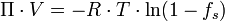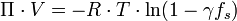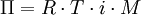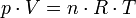- Oncotique
-
Osmose
L’osmose est un mot créé en 1854 par le chimiste écossais Thomas Graham à partir du grec ὠσμός qui signifie « poussée »[1] pour désigner la force qui tend à équilibrer les concentrations moléculaires.
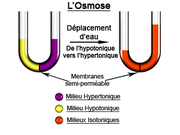
L'osmose est donc définie par sa mise en évidence expérimentale comme le phénomène de diffusion de molécules de solvant (l'eau de façon générale) à travers une membrane semi-perméable qui sépare deux liquides de concentrations en soluté différentes. Le passage de solvant d'un compartiment à l'autre va créer une différence de pression hydrostatique qui va compenser exactement la différence de pression osmotique (cf. ci-après).
Cette notion a permis de mieux comprendre le comportement des solutions aqueuses en chimie, à la fin du XIXe siècle ; mais elle est aussi particulièrement utile en physiologie et en biologie cellulaire pour expliquer les échanges chimiques au sein des organismes vivants.
Sommaire
Historique
En 1748 ou 1749, l'abbé Nollet remarque que lorsque l'on sépare de l'eau et de l'alcool par une vessie animale, l'eau passe dans l'alcool mais jamais l'inverse. Dans ses travaux sur les solutions aqueuses menés entre 1827 et 1832, René Dutrochet propose les termes « d'endosmose » et « d'exosmose » pour désigner ce phénomène. K. Vicrordt s'intéresse également à ce phénomène en 1848. En 1854, Thomas Graham travaille sur les substances colloïdes et découvre qu'elles ne peuvent pas passer à travers une membrane animale.
C'est M. Traube, en 1864, qui conçoit la première membrane artificielle en ferrocyanure de cuivre Cu2Fe(CN)6. En 1877, Wilhelm Friedrich Philipp Pfeffer (1845-1920) fait précipiter le ferrocyanure de cuivre dans un matériau poreux, ce qui permet d'avoir une membrane avec une bonne résistance mécanique.
En 1884, de Vries travaille sur la plasmolyse et la turgescence des cellules végétales.
En 1886, van 't Hoff publie une analogie entre les solutions aqueuses et les gaz parfaits et applique la thermodynamique à l'osmose. Il établit une loi similaire à la loi de Gay-Lussac et propose l'adjectif « semiperméable » pour désigner les membranes. Il reçoit le prix Nobel de chimie en 1901 pour ses travaux.
En 1899, A. Crum Brown utilise trois phases liquides (une solution aqueuse de nitrate de calcium saturée en phénol en bas, couche de phénol pur au milieu et une solution d'eau saturée en phénol en haut). Il remarque un phénomène d'osmose (l'eau passe de la phase du haut vers la phase du bas), la phase liquide du milieu jouant le rôle de membrane semiperméable. Il établit ainsi l'importance de la solubilité de l'espèce diffusante dans la membrane.
Entre 1901 et 1923, H. N. Morse et J. C. W. Frazer mènent un travail systématique de mesure de la perméabilité pour différents précipités gélatineux : des ferrocyanures et des phosphates d'uranyl, de fer, de zinc, de cadmium et de manganèse.
Phénomène
On met en évidence l'osmose par le passage de molécules ou d’ions à travers une membrane, lorsqu’il y a deux solutions de composition différente de chaque côté.
Le phénomène d'osmose nécessite la présence de deux compartiments séparés par une membrane semi-perméable, c’est-à-dire perméable uniquement à l'eau (ou au solvant de façon plus générale) et imperméable aux solutés. Lorsque les deux solutions ne contiennent pas le même nombre de particules dissoutes par unité de volume, on observe un mouvement d'eau qui va tenter de compenser cette différence de concentration en diluant le compartiment le plus concentré.
L’osmose est à l’origine de la turgescence et la plasmolyse de la cellule végétale.
Potentiel chimique
Quand un soluté est dissout dans un solvant, le mélange désordonné des deux espèces produit un accroissement de l'entropie du système qui correspond à une réduction du potentiel chimique. Dans le cas d'une solution idéale la réduction du potentiel chimique est égale à :
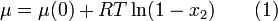
où R est la constante des gaz parfaits, T la température absolue et x2 la concentration du soluté en termes de fraction molaire. La plupart des solutions réelles s'approchent du comportent idéal aux faibles concentrations. Aux hautes concentrations les interactions entre solutés sont la cause d'un écart à l'Équation 1). Ce potentiel chimique réduit induit une force motrice qui est responsable de la diffusion de l'eau à travers la membrane semi-perméable.
Pression osmotique
La pression osmotique se définit comme la pression minimum qu’il faut exercer pour empêcher le passage d’un solvant d’une solution moins concentrée à une solution plus concentrée au travers d’une membrane semiperméable (membrane hémiperméable). En biophysique, on distingue la pression oncotique qui est la part de la pression osmotique due aux protéines. Il faut bien comprendre que la pression osmotique se concrétise quand la part de la fraction molaire du solvant aqueux n'est pas égal à 1.
On pourrait imaginer que, dans la solution la plus concentrée, les molécules d'eau sont en moins grand nombre et que donc il y a égalisation de ce nombre de molécule d'eau de chaque part de la membrane. Mais cet effet est très minime. En fait, dans la solution la plus concentrée, les molécules d'eau (si le solvant est de l'eau) s'agglomèrent autour des molécules de soluté hydrophiles. Ces molécules accaparées ne traversent pas la membrane; l'important c'est la différence de concentration de «l'eau libre». Ainsi l'eau libre se déplace à partir de la solution où la concentration d'eau libre est élevée vers la solution où la concentration d'eau libre est faible, jusqu'à ce que les concentrations soient égales. Mais au bout du compte, le résultat est toujours le même : le solvant se déplace vers la solution dont la concentration de soluté est la plus élevée[2].
La pression osmotique est proportionnelle aux concentrations de soluté de part et d’autre de la membrane et de la température ; lorsque l’on est en présence de plusieurs solutés, il faut prendre en compte la totalité des solutés (à la manière d’un gaz composé, somme des pressions partielles).
La pression osmotique d'une solution idéale se calcule par une formule développée par van't Hoff en 1886 et appliquant le deuxième principe de la thermodynamique.
où
- Π est la pression osmotique, en Pa ;
- V est le volume molaire occupé par le solvant ;
- R est la constante des gaz parfaits ;
- T est la température absolue, en K ;
- fs est la fraction molaire du soluté.
L'équation appliquée aux solutions réelles est, quant à elle,
où γ est le coefficient d'activité du soluté.
Pour une solution très diluée, fs est proche de 0, et − ln(1 − fs) ≈ fs. On peut donc simplifier l'équation en
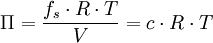 : c'est la loi de van't Hoff
: c'est la loi de van't Hoff
où
- c est la concentration de la solution (en sommant toutes les espèces présentes).
On peut également l'écrire comme ceci :
où
- i est le nombre de particules par entité formulaire
- M est la concentration molaire (moles par litre)
(On appelle i.M la concentration molaire colligative)
On remarque l'analogie avec la loi des gaz parfaits
où
- V est le volume du gaz ;
- n est le nombre de moles de gaz ;
Considérons deux solutions aqueuses 1 et 2 de pressions osmotiques Π1 et Π2, alors si Π1 > Π2, l’eau passe de 2 vers 1 ; 2 se concentre (Π2 augmente) et 1 se dilue (Π1 diminue), jusqu’à égalité entre les pressions osmotiques.
Pression osmotique et pression hydrostatique
La pression osmotique est aussi une pression mécanique, exerçant une force sur la membrane. Si la différence de pression osmotique est très grande, cela peut entraîner la rupture de la membrane (cas de l’hémolyse).
À l’inverse, si l’on exerce une pression mécanique (hydrostatique), on peut forcer le passage d’espèces à travers la membrane. C’est ce qui arrive lors d’un œdème aigu du poumon, et c’est ce que l’on utilise dans l’osmose inverse. Ce phénomène est aussi observable sur les œufs des poissons d'aquarium qui peuvent éclater ou s'écraser selon la différence de pression osmotique de chaque côté de la membrane, la coquille.
L'osmose inverse est une technique de purification de l'eau ; c'est aussi une technique de dessalement de l'eau de mer permettant la production d'eau douce.
Expression commune : Osmose
Le mot osmose, utilisé dans son sens le plus commun, désigne les dégâts visibles sur les revêtements polyester des coques de bateaux, et des piscines. Longtemps considéré comme un défaut de fabrication, il semble que d'infimes particules de Cobalt, excitées par de faibles courant électriques, dus à de mauvaises masses, se colorent d'un brun rougeâtre, tout en provoquant une rupture plus ou moins importante, dans l'étanchéité intrinsèque du matériau polyester. De nos jours, des recherches - toujours en développement - démontrent que si les courants faibles, et la présence de particules de cobalt, ainsi qu'une mauvaise hygrométrie lors de l'application des résines, peuvent aggraver ou déclencher ce phénomène d'osmose, ces facteurs ne permettent pas d'en expliquer l'absence, sur d'autres revêtements polyester pourtant exposés aux mêmes traitements. A ce jour, s'il est devenu possible d'expliquer comment l'osmose prend naissance, il n'est toujours pas été possible d'expliquer pourquoi, certains revêtements sont attaqués et d'autres pas.
Références
- ↑ http://www.cnrtl.fr/etymologie/osmose
- ↑ Campbell, Neil A. et Jane B. Reece, 2007. Biologie. Erpi, Montréal, Canada.
Annexes
Articles connexes
- Dialyse
- Diffusion
- Effet Gibbs-Donnan
- Électro-osmose
- Entropie
- Hypertonique
- Hypotonique
- Osmolalité
- Osmorégulation
- Osmose inverse
- Transport actif
Liens externes
- European Membrane House
- Animation de l'osmose
- Simulation de l’Osmose (Java Applet pour ordinateurs puissants)
- Simulation de l’Osmose (Java Applet pour ordinateurs moins puissants)
Bibliographie
- S. Glasstone, Textbook of physical chemistry 2e éd. (1948), Macmillan Student Edition
- Portail de la chimie
- Portail de la biologie cellulaire et moléculaire
- Portail de la physique
Catégories : Thermodynamique | Physiologie cellulaire | Biophysique | Mécanique des fluides | Biologie des membranes | Chimie des solutions
Wikimedia Foundation. 2010.