- 552-89-6
-
2-nitrobenzaldéhyde
2-nitrobenzaldéhyde 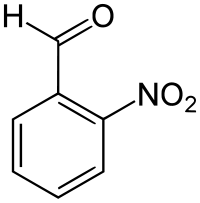
Général Nom IUPAC 2-nitrobenzaldéhyde Synonymes orthonitrobenzaldéhyde
o-nitrobenzaldéhydeNo CAS No EINECS PubChem SMILES InChI Apparence poudre cristalline jaune à l'odeur caractéristique Propriétés chimiques Formule brute C7H5NO3 [Isomères] Masse molaire 151,1195 g∙mol-1
C 55,63 %, H 3,33 %, N 9,27 %, O 31,76 %,Propriétés physiques T° fusion 39,5 °C[1] T° ébullition 153,1 °C (à 0,031 bar[2] Solubilité très peu soluble dans l'eau[3] T° d’auto-inflammation 200 °C[3] Précautions Directive 67/548/EEC 
XnPhrases R : 22, 36/37/38, Phrases S : 26, Écotoxicologie DL50 600mg/kg (souris, oral)[4] LogP 1,74[3] Composés apparentés Isomère(s) 3-nitrobenzaldéhyde
4-nitrobenzaldéhydeUnités du SI & CNTP, sauf indication contraire.
Le 2-nitrobenzaldéhyde, orthonitrobenzaldehyde ou o-nitrobenzaldéhyde est un composé organique aromatique. C'est un dérivé du benzène, substitué par un groupe nitro et un groupe aldéhyde en position ortho, donc l'isomère ortho du nitrobenzaldéhyde.Le 2-nitrobenzaldéhyde est un intermédiaire dans la synthèse de l'indigo appelée synthèse de Baeyer-Drewsen de l'indigo.
Production et synthèse
La synthèse directe du 2-nitrobenzaldéhyde par nitration du benzaldéhyde pose problème, puisque le groupe aldéhyde est un groupe orienteur en meta. Ainsi l'isomère meta (le 3-nitrobenzaldéhyde), est produit à 72% contre 19% pour l'isomère ortho (2-nitrobenzaldéhyde), et 9% pour l'isomère para (4-nitrobenzaldéhyde)[5]. Pour cette raison, cette nitration n'est pas faite directement.
- Une première solution est la mono-nitration du toluène à basse température en 2-nitrotoluène (produit 58% d'isomère ortho, le reste en isomère meta et para)[6]. Le 2-nitrotoluène peut ensuite être oxydé en 2-nitrobenzaldéhyde[7][8].
- Une autre solution consiste à oxyder le 2-nitrostyrène. Pour cela, on effectue une nitration du cinnamaldéhyde dans une solution d'anhydride acétique dans l'acide acétique, menant au 2-nitrocinnamaldéhyde[9]. Celui-ci est oxydé en acide 2-nitrocinnamique puis décarboxylé en 2-nitrostyrène. Le groupe éthylène peut ensuite être oxydé de diverses façons pour produire le 2-nitrobenzaldéhyde[10].
Utilisation
Le 2-nitrobenzaldéhyde est un intermédiaire utilisé dans la synthèse de l' Indigo, colorant insoluble dans l'eau, utilisé couramment pour teindre les jeans et d'autres produits.
La synthèse de Baeyer-Drewsen de l'indigo est une méthode de synthèse initiée par les chimistes allemands Adolf von Baeyer et Viggo Drewsen en 1882. Elle valut le prix Nobel de chimie à Adolf von Baeyer (ainsi que pour ses nombreux autres travaux).
Dans cette synthèse, deux moles de 2-nitrobenzaldéhyde sont condensées sur deux moles d'acétone en milieu basique, donnant une mole d'indigotine (indigo)[11][12][13].
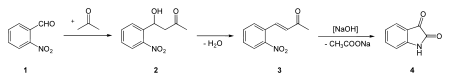
En 1883, Adolf von Baeyer breveta par ailleurs la synthèse de l'isatine (le premier réactif à partir duquel il synthétisa l'indigo) à partir du 2-nitrobenzaldéhyde, reposant sur le même type de réaction que la précédente :
Le 2-nitrobenzaldéhyde peut servir de réactif à de nombreuses autres synthèses organiques, du fait de la réactivité de ses substituants.
Les dérivés de 2-nitrobenzaldéhyde peuvent aussi servir à synthétiser d'autres indigoïdes (dérivés de l'indigo), comme le carmin d'indigo ou le pourpre de Tyr.
Notes et références
- ↑ Hajos, A.,Experiments in the Domain of chloroamphenicols VIII. Preparation of nitroacetophenones and nitrobenzaldehydes and various derivatives through oxidative oxime cleavage,Acta Chim. Acad. Sci. Hung., 1959, 21, 131. - Incertitude attribuée par le Thermodynamics Research Center (NIST Boulder Laboratories, M. Frenkel director) de 1,5 K
- ↑ CRC Handbook of Data on Organic Compounds, 2nd Editon, Weast,R.C and Grasselli, J.G., ed(s)., CRC Press, Inc., Boca Raton, FL, 1989, 1.
- ↑ a , b et c Entrée dans la base de données de produits chimiques GESTIS de la BGIA (organisme allemand responsable de la sécurité et de la santé au travail) ( allemand], anglais]), accès le 06/08/09 (JavaScript nécessaire)
- ↑ Annales des Falsifications et de l'Expertise Chimique. Vol. 76(815), Pg. 65, 1983.
- ↑ Structure of Benzene, California State University Dominguez Hills
- ↑ http://www.thecatalyst.org/experiments/AndersonS/AndersonS.html Product Distribution in the Nitration of Toluene, Steven W. Anderson, January 7, 1999
- ↑ Synthesis of 2-Nitrobenzaldehyde from 2-Nitrotoluene, Alexander Popkov
- ↑ o-Nitrobenzaldehyde. Consulté le 2009-07-21
- ↑ o-NITROCINNAMALDEHYDE, nitration of cinnamaldehyde, organic-synthesis
- ↑ Selective aerobic oxidation of styrene to benzaldehyde catalyzed by water-soluble palladium(II) complex in water, Bo Feng, Zhenshan Hou, Xiangrui Wang, Yu Hu, Huan Li and Yunxiang Qiao
- ↑ Synthesis of Indigo
- ↑ Indigo Synthesis
- ↑ Synthesis of Indigo and Vat Dyeing
- (en) Cet article est partiellement ou en totalité issu d’une traduction de l’article de Wikipédia en anglais intitulé « 2-Nitrobenzaldehyde ».
- Portail de la chimie
Catégories : Produit chimique nocif | Nitrobenzène | Benzaldéhyde
Wikimedia Foundation. 2010.