- Oxétane
-
Oxétane 
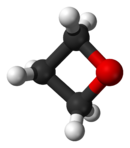
Général Nom IUPAC oxétane Synonymes oxyde de 1,3-propylène
1,3-époxypropane
oxacyclobutane
oxyde de triméthylèneNo CAS No EINECS ChEBI SMILES InChI Propriétés chimiques Formule brute C3H6O [Isomères] Masse molaire[1] 58,0791 ± 0,0031 g·mol-1
C 62,04 %, H 10,41 %, O 27,55 %,Propriétés physiques T° fusion -97 °C [2] T° ébullition 48 °C [2] Solubilité 1 000 g·l-1 (eau,20 °C) [3] Masse volumique 0,8930 g·cm-3 à 25 °C [2] Point d’éclair -37 °C [2] Limites d’explosivité dans l’air 2,4 - ? Vol.% [2] Pression de vapeur saturante 324 mmHg à 25 °C [3] Thermochimie ΔfH0gaz -80,54 kJ·mol-1 ΔvapH° 30,21 kJ·mol-1 [4] Cp 99,6 J·K-1·mol-1 (liquide,24,85 °C)
61,5 J·K-1·mol-1 (gaz,25 °C)[4]PCI -1 957,5 kJ·mol-1 (gaz) [4] Propriétés optiques Indice de réfraction  1.3905[5]
1.3905[5]Précautions Directive 67/548/EEC[6] 
Xn
FPhrases R : 11, 20/21/22, Phrases S : 2, 9, 16, 26, 29, Transport[2] 33/30 1993 NFPA 704[7] Écotoxicologie DL50 0,5 g·kg-1 (rat, s.c.) [3] LogP -0,14 [2] Unités du SI & CNTP, sauf indication contraire. L'oxétane ou l'1,3-époxypropane est un composé organique hétérocyclique de formule brute C3H6O qui consiste en un cycle à quatre atomes, trois de carbone et un d'oxygène.
Plus généralement, le terme oxétane réfère aussi tout composé organique qui contient un cycle oxétane.
Préparation
Une méthode de préparation bien connue et typique est la réaction de l'hydroxyde de potassium sur l'acétate de 3-chloropropyle à 150 °C[5]. Le rendement d'oxétane fait par cette voie est d'environ 40 % parce que cette synthèse peut évidemment conduire à un grand nombre de sous-produits.
D'autres réactions pour préparer de l'oxétane sont la réaction de Paternò-Büchi ou une cyclisation de diol qui peut aussi former un cycle oxétane.
Taxol
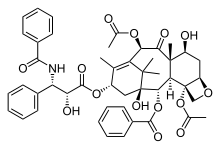 Paclitaxel avec un cycle oxétane à droite.
Paclitaxel avec un cycle oxétane à droite.
Le paclitaxel (Taxol) est un exemple d'un produit naturel contenant un cycle oxétane. Le Taxol est devenu un centre d'intérêt majeur pour de nombreux chercheurs en raison de sa structure inhabituelle et de ses propriétés d'anti-cancéreux[8]. Son cycle oxétane est une caractéristique importante qui sert dans son activité structurelle de fixation des microtubules. Cependant peu est connu sur la façon dont la réaction est catalysée naturellement, ce qui est un défi pour les scientifiques qui tentent de reproduire cette réaction[8].
Notes
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Oxetane » (voir la liste des auteurs)
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- Entrée de « 1,3-Propylene oxide » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 9 fövrier 2010 (JavaScript nécessaire)
- (en) « 503-30-0 » sur ChemIDplus, consulté le 9 février 2010
- (en) « Oxetane » sur NIST/WebBook, consulté le 9 février 2010
- C. R. Noller, "trimethylene oxide", Org. Synth., 1955, Coll. Vol. 3, p. 835.
- « 1,2-époxypropane » sur ESIS, consulté le 9 février 2010
- UCB Université du Colorado
- Willenbring, Dan, and Dean J. Tantillo, "Mechanistic possibilities for oxetane formation in the biosynthesis of Taxol’s D ring.", Russian Journal of General Chemistry, 2008, vol. 78(4), pp.723-731.
Catégories :- Produit chimique nocif
- Produit chimique facilement inflammable
- Oxétane
Wikimedia Foundation. 2010.


