- Formamide
-
Formamide 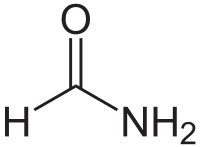
Général Nom IUPAC Formamide Synonymes méthanamide
CarbamaldéhydeNo CAS No EINECS SMILES InChI Apparence liquide incolore, hygroscopique, visqueux[1]. Propriétés chimiques Formule brute CH3NO [Isomères] Masse molaire[4] 45,0406 ± 0,0015 g·mol-1
C 26,67 %, H 6,71 %, N 31,1 %, O 35,52 %,pKa 0,3 Moment dipolaire 3,73 ± 0,07 D [2] Diamètre moléculaire 0,431 nm [3] Propriétés physiques T° fusion 2,5 °C[1] T° ébullition (décomposition) : 210 °C[1] Solubilité dans l'eau : très bonne[1],
bonne dans l'éthanol
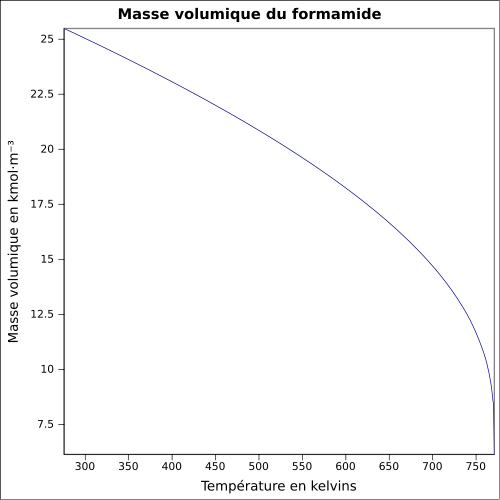
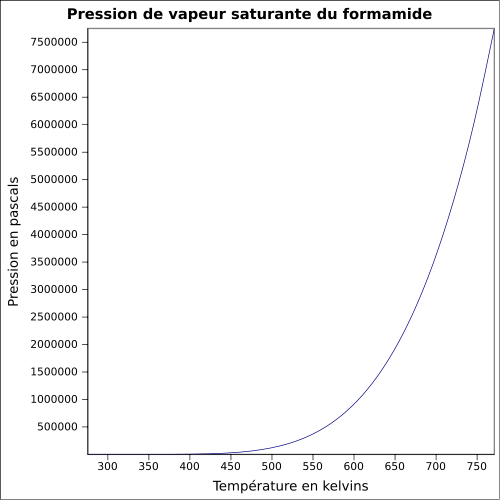
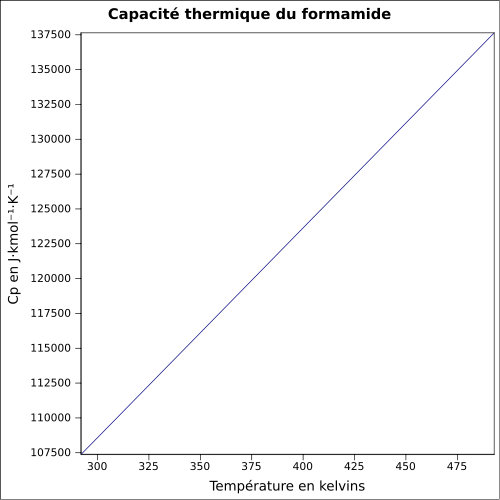
peu soluble dans les solvants polaires.Masse volumique 1,1334 g·cm-3 [5] T° d'auto-inflammation >500 °C[1] Point d’éclair 154 °C (coupelle ouverte)[1] Pression de vapeur saturante à 20 °C : environ 2 Pa[1] Thermochimie Cp Propriétés électroniques 1re énergie d'ionisation 10,16 ± 0,06 eV (gaz)[8] Propriétés optiques Indice de réfraction  1,446 [3]
1,446 [3]Précautions Directive 67/548/EEC 
TPhrases R : 61, Phrases S : 45, 53, NFPA 704 Unités du SI & CNTP, sauf indication contraire. Le formamide est un amide provenant de l'acide formique. À température ambiante, il se présente comme un liquide incolore proche de la consistance de la glycérine. C'est un solvant hygroscopique et un réducteur d'odeur proche de celle de l'ammoniac. Il peut se transformer en acide cyanhydrique s'il est soumis à des températures supérieures à 90 °C. À des températures supérieures à 200 °C, le formamide se transforme en acide cyanhydrique, ammoniac, monoxyde de carbone et eau.
Sommaire
Données physiques complémentaires
densité de vapeur: 1,55 (air = 1)
pression de vaporisation: 0,08 mmHg (11 Pa) à 20 °C
point éclair: 154 °C
pKa: 23,5Production
La réaction entre l'acide formique et l'ammoniac produit du formiate d'ammonium, lequel peut conduire sous l'action de la chaleur au formamide :
- HCOONH4 → HCONH2 + H2O
Utilisations
Le formamide est utilisé dans les applications suivantes:
- Synthèse des vitamines ;
- Acide prussique ;
- Acide cyanhydrique ;
- Colles ;
- Déstabilisation des acides nucléiques (rupture des liaisons hydrogènes entre les bases) ;
- Synthèse du 3,4-méthylènedioxyamphétamine (MDA) ;
- Tampon favorisant la séparation et l'ionisation de composés apolaires dans les techniques séparatives analytiques, par exemple : Chromatographie en phase liquide couplée à la Spectrométrie de Masse en Tandem (HPLC - ESI -MS/MS);
Voir aussi
Liens externes
- http://www.reptox.csst.qc.ca/Produit.asp?no_produit=3731 (CSST - Service du répertoire toxicologique)
- http://docs.appliedbiosystems.com/pebiodocs/00102922.pdf (consignes de sécurité).
- http://www.cdc.gov/niosh/ipcsnfrn/nfrn0891.html (Fiches internationales de Sécurité chimique).
- http://chemsub.online.fr/name/formamide.html (ChemSub Online : Formamide.)
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « formamide » (voir la liste des auteurs)
- (de) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en allemand intitulé « formamid » (voir la liste des auteurs)
Notes et références
- FORMAMIDE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- (en) David R. Lide, Handbook of chemistry and physics, CRC, 16 juin 2008, 89e éd., 2736 p. (ISBN 142006679X et 978-1420066791), p. 9-50
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, England, John Wiley & Sons Ltd, 1999, 239 p. (ISBN 0-471-98369-1)
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- (en) J. G. Speight, Norbert Adolph Lange, Lange's handbook of chemistry, McGraw-Hill, 2005, 16e éd., 1623 p. (ISBN 0071432205), p. 2.289
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, 1997, 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 1, 2 et 3, Huston, Texas, Gulf Pub. Co., 1996 (ISBN 0-88415-857-8, ISBN 0-88415-858-6, ISBN 0-88415-859-4)
- (en) David R. Lide, Handbook of chemistry and physics, CRC, 2008, 89e éd., 2736 p. (ISBN 9781420066791), p. 10-205
Catégories :- Produit chimique toxique
- Produit chimique reprotoxique
- Amide
Wikimedia Foundation. 2010.