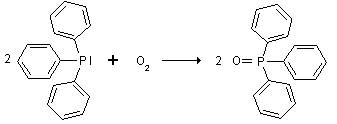- Triphenylphosphine
-
Triphénylphosphine
Triphénylphosphine 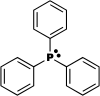
Formule de la Triphénylphosphine Général Nom IUPAC Triphenylphosphane No CAS No EINECS SMILES InChI Apparence cristaux blancs sans odeur.[1] Propriétés chimiques Formule brute C18H15P [Isomères] Masse molaire 262,2855 g∙mol-1
C 82,43 %, H 5,76 %, P 11,81 %,Propriétés physiques T° fusion 80 °C[1] T° ébullition 377 °C[1] Solubilité dans l'eau : nulle[1] Masse volumique 1,1 g∙cm-3 Point d’éclair 180 °C c.o.[1] Précautions Directive 67/548/EEC 
XnPhrases R : 22, 43, 53, Phrases S : 24, 37, 61, NFPA 704 Écotoxicologie DL50 700 mg/kg (rats, oral) Valeur d'exposition 5 mg/m³ Unités du SI & CNTP, sauf indication contraire. La triphénylphosphine (ou triphénylphosphane), est un composé organophosphoré de formule P(C6H5)3 - parfois abrégé en PPh3 or Ph3P. Il est largement utilisé dans la synthèse de composés organiques et d'organométalliques. C'est un composé relativement stable qui existe sous la forme d'un solide cristallin à température ambiante et qui se dissout dans les solvants non-polaires comme le benzène.
Sommaire
Préparation
Même si elle n'est pas chère, la triphénylphosphine peut être préparée en laboratoire par traitement du trichlorure de phosphore avec le bromure de phénylmagnésium ou le phényllithium. La synthèse industrielle met en jeu la réaction de Friedel-Crafts entre le trichlorure de phosphore et le benzène. La triphénylphosphine peut être recristallisée soit dans l'éthanol chaud soit dans l'isopropanol chaud. Cette purification est parfois conseillée pour enlever l'oxyde de triphénylphosphine, de formule OP(C6H5)3, qui s'est formé par oxydation lente par l'air.
Principales réactions organiques
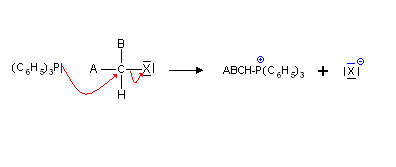
P(C6H5)3 est largement utilisé en synthèse organique. La réaction du P(C6H5)3 sur les halogénoalcanes conduit à des sels phosphoriques appelés aussi sels de phosphonium.
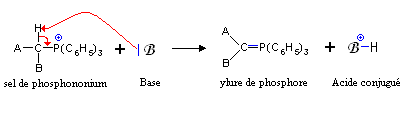
Ces sels réagissent avec des bases fortes (type organométalliques par exemple les organolithiens, ions amidures -NH2- ou hydrure H-, des bases moins fortes pouvant être utilisées dans certain cas) pour former des ylures de phosphore, appelés aussi phosphoranes.
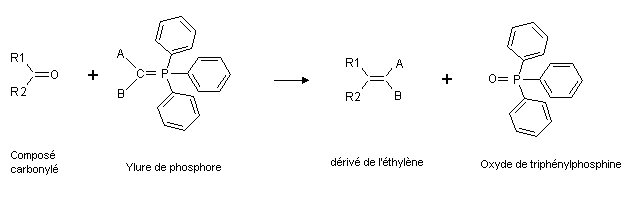
Ces molécules sont utilisées en particulier dans la Réaction de Wittig, où, créees in situ, elles réagissent avec des composés carbonylés, aldéhydes ou cétones, pour former des dérivés éthylèniques, voire des alcènes.
réaction de Wittig réaction de Wittig La réaction de P(C6H5)3 sur les chlorines donne Cl2P(C6H5)3, crée in situ pour transformer les alcools en dérivés chlorés , formant par la même occasion HCl et un oxyde de tryphénylphosphine O=P(C6H5)3.
Réactions avec les composés inorganiques et les organométalliques
La triphénylphosphine est souvent utilisée comme ligand d'un cation métallique pour former un complexe de coordination. Elle se lie à la plupart des métaux de transition, en particulier aux métaux du milieu et de la fin du bloc d comme le palladium, le platine, le ruthénium, le nickel et l'osmium. Exemple : le Tetrakis(triphenylphosphine) de palladium(0). Les triphénylamines correspondantes ont une faible affinité pour les métaux de transition. Cette différence s'explique par la plus petite taille de l'atome d'azote, ce qui entraîne une plus grande gène stérique limitant l'approche du ligand vers le centre métallique.
Les composés de type metal-P(C6H5)3 sont caractérisés par spectroscopie RMN du 31P.
La triphénylphosphine capte le soufre à partir de nombreux composés sulfurés, y compris du soufre élémentaire. Le produit phosphoré est SP(C6H5)3. Cette réaction peut être utilisée pour analyser les taux de soufre.
Utilisation en chimie organophosphorique
La triphénylphosphine est couramment employée comme précurseur pour d'autres organophosphines. Du lithium dans du THF et du sodium (Na) ou potassium (K) dans de l'ammoniaque NH3 réagissent pour donner (C6H5)2PM (M = Li, Na, K). Un des défauts de ces réactions est de générer autant de phényllithium (ou sodium, ou potassium) C6H5M, mais ces espèces peuvent être sélectivement converties en benzène par utilisation attentive d'acide. Le traitement du diphénylphosphure de métal alcalin par un agent d'alkylation RX donne PRC6H5)2. Cette méthode peut être utilisée pour préparer des ligands comme PMe(C6H5)2 (methyldiphenylphosphine). La réaction avec les dihalogénoalcanes correspondante donne des bis(diphénylphosphino)alcanes. Par exemple, le dibromure d'éthylène et Ph2PM réagissent pour donner (C6H5)2PCH2CH2P(C6H5)2, appelé 1,2-bis(diphénylphosphino)éthane ou dppe. L'addition d'acide, même faibles comme le chlorure d'ammonium, convertit (C6H5)2PM en (C6H5)2PH, ou diphénylphosphine.
La sulfonation de P(C6H5)3 donne la tris(3-sulfophényl)phosphine, P(C6H4-3-SO3-)3. Cette phosphine anionique est habituellement isolée comme sel de trisodium et est connu comme TPPTS. Contrairement à P(C6H5)3, TPPTS est soluble dans l'eau, comme ses dérivés métalliques. Les complexes TPPTS de rhodium sont utilisés dans certaines réactions industrielles d'hydroformylation en raison d'un catalyseur hydrosoluble séparable des composés organiques.
Autres réactions impliquant des triphénylphosphines :
- réaction d'Appel
- réaction de Mitsunobu
- réaction de Wittig
- réaction de Staudinger
- comme ligand dans la réaction de Heck
- Dans la production du catalyseur de Wilkinson et du complexe de Vaska
Liens externes
Notes et références
- ↑ a , b , c , d et e TRIPHENYLPHOSPHINE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- Portail de la chimie
Catégories : Composé du phosphore | Produit chimique nocif | Produit chimique dangereux pour l'environnement | Composé aromatique
Wikimedia Foundation. 2010.