- Triclosan
-
Triclosan 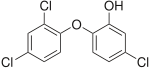
Général Nom IUPAC 5-chloro-2-(2,4-dichlorophénoxy)phénol No CAS No EINECS PubChem SMILES InChI Apparence poudre blanche Propriétés chimiques Formule brute C12H7Cl3O2 [Isomères] Masse molaire[1] 289,542 ± 0,017 g·mol-1
C 49,78 %, H 2,44 %, Cl 36,73 %, O 11,05 %,Propriétés physiques T° fusion 54 à 57,3 °C T° ébullition >280 °C décomposition Solubilité 10 mg·l-1 eau à 20 °C Point d’éclair 223 °C Précautions Directive 67/548/EEC 
Xi
NPhrases R : 36/38, 50/53, Phrases S : 26, 39, 46, 60, 61, SGH[2] 

AttentionÉcotoxicologie DL50 3 700 mg·kg-1 rat oral
29 mg·kg-1 rat i.v.
3 900 mg·kg-1 rat s.c.
89 mg·kg-1 rat i.p.Unités du SI & CNTP, sauf indication contraire. Le triclosan est un agent antifongique et antibactérien à large spectre. Il est aussi appelé 5-chloro-2-(2,4-dichlorophénoxy)phénol.
On le trouve dans des savons, des déodorants, des dentifrices et beaucoup de produits de consommation courante sont imprégnés de triclosan : ustensiles de cuisine, jouets, literie, sacs poubelle...[3] Il diminue la contamination bactérienne sur les mains et les produits traités.
Le triclosan a été suspecté de causer le développement de bactéries plus résistantes. Mais aucune étude n'a pu prouver cet effet à ce jour.
Des études ont montré que le triclosan peut se combiner avec le chlore pour former du chloroforme[4] gazeux. Les conditions nécessaires à cette réaction chimique exigent un excès significatif de chlore ainsi qu’une forte concentration de triclosan.
Le triclosan fait partie des perturbateurs endocriniens. Ce composé est suspecté, à partir d'une concentration encore méconnue, de bloquer la fabrication d'œstrogène, ce qui peut s'avérer particulièrement dangereux pour la femme enceinte, le développement cérébral et l'oxygénation du fœtus[5]. Ses effets ont aussi été observés chez les amphibiens (Rana catesbeiana, Xenopus laevis). Il a montré une toxicité chronique et aiguë chez les espèces aquatiques. En outre, le triclosan est bioaccumulatif[6].
Le triclosan est le biocide qui fait l’objet du plus grand nombre d’études concernant la résistance aux antimicrobiens, notamment son action sur les bactéries et les mécanismes de résistance microbienne. Le Comité scientifique pour la sécurité des consommateurs (CSSC) en conclut qu’à ce jour, rien ne prouve que l’utilisation du triclosan entraîne une augmentation de la résistance aux antibiotiques. Cependant, il est trop tôt pour dire que l’exposition au triclosan ne donne jamais lieu à une résistance microbienne, car l’on ne dispose pas d’informations suffisantes pour faire une analyse exhaustive des risques.[7]
Voir aussi
Références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- Le 5-chloro-2-(2,4-dichlorophenoxy)phénol – vous connaissez? sur le site Agence Science-Presse.
- Le chloroforme est classé comme probable cancérigène.
- Antibacterial agent could cause pregnancy problems
- Jackson J, Sutton R, Sources of endocrine-disrupting chemicals in urban wastewater, Oakland, CA, Sci. Total Environ. (2008), doi:10.10116/j.scitotenv.2008.06.033
- Triclosan et la résistance aux antibiotiques résumé par GreenFacts d'un rapport scientifique du Comité scientifique pour la sécurité des consommateurs de la Commission européenne(CSSC)
Catégories :- Produit chimique irritant
- Produit chimique dangereux pour l'environnement
- Chlorobenzène
- Dichlorobenzène
- Phénol
- Phénoxybenzène
- Antibiotique
- Antimycosique
Wikimedia Foundation. 2010.
