- Nitrométhane
-
Nitrométhane 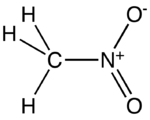
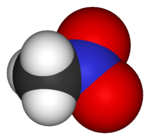
Général Nom IUPAC Nitrométhane No CAS No EINECS Apparence liquide visqueux incolore, d'odeur caractéristique[1]. Propriétés chimiques Formule brute CH3NO2 [Isomères] Masse molaire[4] 61,04 ± 0,0018 g·mol-1
C 19,68 %, H 4,95 %, N 22,95 %, O 52,42 %,Moment dipolaire 3,46 ± 0,02 D[2] Diamètre moléculaire 0,449 nm[3] Propriétés physiques T° fusion -29 °C[1] T° ébullition 101 °C[1] Masse volumique 1,137 g·cm-3[5],
2.11 (vapeur)T° d'auto-inflammation 417 °C[1] Point d’éclair 35 °C (coupelle fermée)[1] Limites d’explosivité dans l’air 7,3–60 %vol[1] Point critique 63,1 bar, 314,85 °C[6] Point triple 244,77 K (-28,38 °C) Thermochimie ΔfH0gaz -81 kJ/mol ΔfH0liquide -113 kJ/mol Cp 106 J/mol.K (liquide) Chaleur latente
de vaporisation34 kJ/mol Chaleur latente
de fusion9,7 kJ/mol Propriétés électroniques 1re énergie d'ionisation 11,08 ± 0,07 eV (gaz)[8] Propriétés optiques Indice de réfraction  1,379[3]
1,379[3]Précautions Directive 67/548/EEC 
XnPhrases R : 5, 10, 22, Phrases S : (2), 41, Transport - 1261 NFPA 704 SGH[10] 

AttentionClassification du CIRC Groupe 2B : Peut-être cancérogène pour l'homme[9] Écotoxicologie Seuil de l’odorat bas : 3,5 ppm
haut : 100 ppm[11]Unités du SI & CNTP, sauf indication contraire. Le nitrométhane est un composé organique dont la formule chimique est CH3NO2. Il est le plus simple composé organique nitré. Il s'agit d'un liquide visqueux, hautement polaire habituellement utilisé comme solvant dans les applications industrielles, comme les extractions, en tant que réactif ou solvant de nettoyage. En tant qu'intermédiaire dans la synthèse organique, il est très utilisé dans la fabrication de produits pharmaceutiques, pesticides, explosifs et fibres. Il est également utilisé comme carburant à haut potentiel pour les véhicules de course et, mélangé à des huiles, dans le modélisme.
Sommaire
Préparation
Le nitrométhane peut être synthétisé par réaction du chloroacétate de sodium avec le nitrite de sodium en solution aqueuse :
- ClCH2COONa + NaNO2 + H2O → CH3NO2 + NaCl + NaHCO3
Il est extrait du mélange réactionnel par distillation.
À l'échelle industrielle, il est produit par nitration du méthane en faisant réagir en phase vapeur le méthane et l'acide nitrique.
Applications
Le nitrométhane est un solvant couramment utilisé en chimie organique[12].
Carburant
Le nitrométhane est utilisé comme carburant pour les véhicules de course, en particulier pour les dragsters, afin de fournir plus de puissance[13]. Il est également utilisé comme comburant, pour donner un apport en oxygène dans les moteurs thermiques de voitures et avions radiocommandés. Dans ces deux cas, il est souvent simplement surnommé nitro.
L'oxygène contenu par le nitrométhane lui permet de brûler avec beaucoup moins d'apport d'oxygène atmosphérique que d'autres hydrocarbures, comme l'essence par exemple. La réaction de combustion est la suivante :
- 4CH3NO2 + 3O2 → 4CO2 + 6H2O + 2N2
14,6 kg d'air sont requis pour la combustion d'un kg d'essence, mais seulement 1,7 kg sont requis pour un kg de nitrométhane. Comme le cylindre d'un moteur ne peut contenir qu'une quantité limitée d'air à chaque cycle, on peut donc brûler 8,7 fois plus de nitrométhane que d'essence. Cependant, le nitrométhane a une densité énergétique inférieure à celle de l'essence (11.3 MJ/kg pour le nitrométhane contre 42 à 44 MJ/kg pour l'essence. Ceci permet de déduire que le nitrométhane génère environ 2,3 fois plus d'énergie que l'essence lorsqu'il est combiné avec un volume d'oxygène donné.
Le nitrométhane peut aussi être utilisé comme monergol, car il peut se décomposer suivant la réaction :
- 4CH3NO2 → 4CO + 4H2O + 2H2 + 2N2
Notes et références
- NITROMETHANE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- (en) David R. Lide, Handbook of chemistry and physics, CRC, 16 juin 2008, 89e éd., 2736 p. (ISBN 142006679X et 978-1420066791), p. 9-50
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, England, John Wiley & Sons Ltd, 1999, 239 p. (ISBN 0-471-98369-1)
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- (en) J. G. Speight, Norbert Adolph Lange, Lange's handbook of chemistry, McGraw-Hill, 2005, 16e éd., 1623 p. (ISBN 0071432205), p. 2.289
- Properties of Various Gases sur flexwareinc.com. Consulté le 12 avril 2010
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 1, 2 et 3, Huston, Texas, Gulf Pub. Co., 1996 (ISBN 0-88415-857-8, ISBN 0-88415-858-6, ISBN 0-88415-859-4)
- (en) David R. Lide, Handbook of chemistry and physics, CRC, 2008, 89e éd., 2736 p. (ISBN 9781420066791), p. 10-205
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 2B : Peut-être cancérogènes pour l'homme » sur http://monographs.iarc.fr, CIRC, 16 janvier 2009. Consulté le 22 août 2009
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- Nitromethane sur hazmap.nlm.nih.gov. Consulté le 14 novembre 2009
- Coetzee, J. F. and Chang, T. H., « Recommended Methods for the Purification of Solvents and Tests for Impurities: Nitromethane », dans International Union of Pure and Applied Chemistry, vol. 58, 1986, p. 1541-1545 [texte intégral]
- K. Owen and T. Coley, Automotive Fuels Reference Book - 2nd edition, Chapter 13 "Racing Fuels", (ISBN 1-56091-589-7) (1995)
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Nitromethane » (voir la liste des auteurs)
Liens externes
- (fr) Fiche toxicologique de l'INRS
- (en) Fiche Nitrométhane sur le WebBook de chimie du NIST
Wikimedia Foundation. 2010.




