- Indigotine
-
Indigo (teinture)
 Pour les articles homonymes, voir indigo (homonymie).
Pour les articles homonymes, voir indigo (homonymie).Indigotine 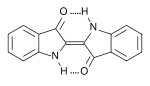
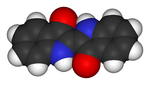
Général Nom IUPAC 2-(1,3-dihydro-3-oxo-2H-indole-2-ylidène)-1,2-dihydro-3H-indole-3-one No CAS No EINECS Apparence Poudre bleu foncé Propriétés chimiques Formule brute C16H10N2O2 [Isomères] Masse molaire 262,2628 g∙mol-1
C 73,27 %, H 3,84 %, N 10,68 %, O 12,2 %,Propriétés physiques T° fusion 390 à 392 °C (sublimation) Solubilité insoluble dans l'eau, l'éthanol ou l'éther à 20 °C Précautions Directive 67/548/EEC 
XiPhrases R : 36/37/38, Phrases S : 26, 36, Unités du SI & CNTP, sauf indication contraire.
L'indigo est le colorant provenant de l'indigotier et servant principalement à la teinture des tissus (les jeans, à leur origine). La molécule colorante est l'indigotine.Sommaire
Chimie
L'indigo(tine) se présente sous la forme d'une poudre cristalline bleu foncé qui se sublime entre 390 °C et 392 °C. Elle est insoluble dans l'eau, l'éthanol ou l'éther, mais soluble dans le chloroforme, le nitrobenzène ou l'acide sulfurique concentré.
La substance est naturellement présente dans l'indican, substance incolore et soluble dans l'eau. L'indican peut facilement être hydrolisé en β-D-glucose et indoxyle. Une oxydation douce, par exemple une simple exposition à l'air, transforme l'indoxyle en indigo.
Le procédé de manufacture développé à la fin des années 1800 est toujours en usage aujourd'hui à travers le monde. Dans ce procédé, l'indoxyle est synthétisé par fusion du phenylglycinate de sodium dans un mélange d'hydroxyde de sodium et de sodamide.
En 1882, Adolf von Baeyer et Viggo Drewsen proposent la première méthode de synthèse de l'indigotine à partir du 2-nitrobenzaldéhyde et de l'acétone. Cette méthode est restée sous le nom de et synthèse de Baeyer-Drewsen de l'indigo.
Plusieurs composés plus simples peuvent être produits par décomposition de l'indigo, notamment l'aniline et l'acide picrique. La seule réaction chimique réellement utile en pratique est la réduction de l'indigo par l'urée en indigo blanc. L'indigo blanc est ensuite ré-oxydé en indigo après avoir été appliqué au produit.
L'indigo traité par l'acide sulfurique produit une couleur bleu-verte. Cette couleur est apparu durant le XVIIIe siècle et a été désignée sous le nom de bleu de Saxe ou carmin d'indigo.
L'indigo a aussi une structure quasi identique au pourpre de Tyr. Seuls deux atomes de brome différencient le 6,6′-dibromoindigo (molécule du pourpre de Tyr) de l'indigo.
Histoire
Une version de l'histoire veut que ce colorant naturel importé en Europe depuis les colonies du nouveau monde ait supplanté le pastel et ainsi ruiné les économies européennes qui en dépendaient (sud-ouest de la France notamment). Or au Moyen-Âge, un bleu (bleu de Prusse, proche de l'indigo) d'origine minérale, était très répandu. La ruine des « pieds bleus », ces teinturiers qui teignaient les vêtements en les foulant, est simplement venue de la mode de la dentelle blanche qui avait remplacé celle des tissus aux couleurs vives.
Cette galerie de photo montre que l'indigo est un bleu foncé et qu'il ne contient pas de trace de violet.
Colorant extrait de l'indigotier déposé sur une feuille de papier.
Pavé d'extrait d'indigo séché provenant de l'Inde.
Jean-Baptiste du Tertre Histoire générale des Antilles (1667)
Notes et références
Voir aussi
- Portail de la chimie
Catégories : Produit chimique irritant | Pigment | Composé indolé
Wikimedia Foundation. 2010.




