- Chlorure de sulfuryle
-
Chlorure de sulfuryle 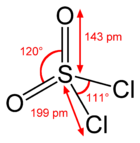

Structure du chlorure de sulfuryleGénéral Nom IUPAC Chlorure de sulfuryle Synonymes Chlorure sulfurique No CAS No EINECS Propriétés chimiques Formule brute SO2Cl2 Masse molaire[1] 134,97 ± 0,01 g·mol-1
Cl 52,53 %, O 23,71 %, S 23,76 %,Propriétés physiques T° fusion -54,1 °C T° ébullition 69,4 °C Masse volumique 1 667 kg·m-3 à 20 °C Précautions Directive 67/548/EEC 
CPhrases R : 14, 34, 37, Phrases S : (1/2), 26, 45, Unités du SI & CNTP, sauf indication contraire. Le chlorure de sulfuryle est un composé chimique de formule SO2Cl2. Il se présente comme un liquide incolore à odeur piquante. On ne le trouve pas dans la nature, en raison de son hydrolyse très rapide.
On le confond souvent avec le chlorure de thionyle SOCl2, mais ces deux oxychlorures de soufre ont des propriétés différentes : le chlorure de thionyle produit des ions chlorures Cl– tandis que le chlorure de sulfuryle donne du chlore Cl2.
Sommaire
Préparation et réactions
On prépare le chlorure de sulfuryle en faisant réagir du dioxyde de soufre SO2 et du chlore Cl2 en présence d'un catalyseur, tel que du charbon actif :
Le produit obtenu peut ensuite être purifié par distillation fractionnée.
Le chlorure de sulfuryle réagit violemment avec l'eau en libérant du chlorure d'hydrogène HCl et en donnant de l'acide sulfurique H2SO4 :
Il se décompose à la chaleur, vers 100 °C, soit environ 30 °C au-dessus de son point d'ébullition. Il se décompose également lentement à température ambiante pour donner du dioxyde de soufre SO2 et du dichlore Cl2, à l'origine de la légère teinte jaunâtre des échantillons de chlorure de sulfuryle qui ont eu le temps de « vieillir ».
Applications
Dans la mesure où le chlorure de sulfuryle est liquide, on le trouve plus commode à manipuler que le dichlore, qui est gazeux, ce qui fait qu'on l'utilise comme source de chlore facilement transportable, stockable et mesurable. Il est également utilisé pour chlorer alcanes, alcènes, alcynes, arènes et époxydes, selon des réactions radicalaires initées par l'AIBN. Il peut en outre convertir les alcools en organochlorés.
Dans l'industrie, le chlorure de sulfuryle intervient surtout dans la fabrication de pesticides.
Sécurité
Le chlorure de sulfuryle est un produit toxique, corrosif et lacrymogène. Il est susceptible de former des mélanges explosifs avec l'eau, ainsi qu'avec le diméthylsulfoxyde O=S(CH3)2 (DMSO) et le diméthylformamide OHC–N(CH3)2 (DMF).
Notes et références de l'article
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
Catégories :- Produit chimique corrosif
- Composé du soufre
- Chlorure
Wikimedia Foundation. 2010.
