- Fluorure de chlorosulfonyle
-
Fluorure de chlorosulfonyle 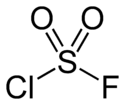
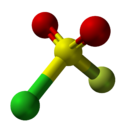
Structure du fluorure de chlorosulfonyle.Général No CAS No EINECS No RTECS PubChem ChEBI SMILES InChI Apparence gaz incolore. Propriétés chimiques Formule brute FSO2Cl Masse molaire[1] 118,515 ± 0,008 g·mol-1
Cl 29,91 %, F 16,03 %, O 27 %, S 27,06 %,Propriétés physiques T° fusion -124,7 °C T° ébullition 7,1 °C Solubilité hydrolyse Masse volumique 1,623 g·cm-3 Précautions Directive 67/548/EEC[2] 
TPhrases R : 14, 23/24/25, 34, Phrases S : 26, 27, 28, 36/37/39, 45, Transport[2] - 2922 SGH[2] 

DangerUnités du SI & CNTP, sauf indication contraire. Le fluorure de chlorosulfonyle est un composé chimique de formule SO2ClF utilisé comme solvant pour composés très oxydants.
Au laboratoire, sa préparation commence par celle de fluorosulfite de potassium KSO2F[3] :
- SO2 + KF → chloré en fluorure de chlorosulfonyle[4] :
- KCl
Le mélange de fluorure de sulfuryle SO2F2.
Le fluorure de chlorosulfonyle peut également être préparé à partir de substance non gazeuses en traitant le chlorure de sulfuryle SO2Cl2 avec du fluorure d'ammonium NH4F ou du fluorure de potassium KF dans de l'acide trifluoroacétique CF3COOH[5] :
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- SIGMA-ALDRICH
- (en) F. Seel, Ralph G. Czerepinski et George H. Cady, « Potassium Fluorosulfite: (Potassium Fluorosulfinate) », dans Inorg. Synth., vol. 9, 1967 [texte intégral, lien DOI (pages consultées le 15 novembre 2010)]
- (en) F. Seel, Leonard C. Duncan, Ralph G. Czerepinski et George H. Cady, « Sulfuryl Chloride Fluoride and Sulfuryl Fluoride », dans Inorg. Synth., vol. 9, 1967 [texte intégral, lien DOI (pages consultées le 15 novembre 2010)]
- (en) V. Prakash Reddy, Donald R. Bellew et G. K. Surya Prakash, « A convenient preparation of sulfuryl chloride fluoride », dans J. Fluor. Chem., vol. 56, no 2, février 1992, p. 195-197 (ISSN 0022-1139) [texte intégral, lien DOI (pages consultées le 15 novembre 2010)]
Catégories :- Produit chimique toxique
- Produit chimique corrosif
- Fluorure
- Chlorure de sulfonyle
- SO2 + KF → chloré en fluorure de chlorosulfonyle[4] :
Wikimedia Foundation. 2010.

