- 78110-38-0
-
Aztréonam
Aztréonam 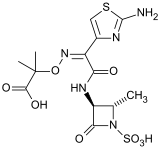
Représentation plane de l'Aztréonam Général Nom IUPAC Acide (Z)-2-[[[(2-amino-4-thiazolyl)[[(2S,3S)-2-méthyl-4-oxo-1-sulfo-3-azétidinyl] carbamoyl]méthylène]amino]oxy]-2-méthylpropionique No CAS No EINECS Code ATC J01 DrugBank PubChem SMILES InChI Apparence Solide Propriétés chimiques Formule brute C13H17N5O8S2 [Isomères] Masse molaire 435,433 g∙mol-1
C 35,86 %, H 3,94 %, N 16,08 %, O 29,39 %, S 14,73 %,pKa -0,7 ; 2,75 ; 3,91 Précautions Directive 67/548/EEC Phrases S : 22, 24/25, Écotoxicologie DL50 >10000 mg/kg souris oral
1963 mg/kg souris i.v.
3906 mg/kg souris s.c.
2897 mg/kg souris i.p.Données pharmacocinétiques Biodisponibilité 100% (injection intramusculaire) Liaison protéique 56% Métabolisme hépatique Demi-vie d’élim. 1,7 heure Excrétion reinale Unités du SI & CNTP, sauf indication contraire. Sommaire
Présentation
Il s'agit d'un agent anti-bactérien de la classe des monobactames. L’aztréonam est le premier représentant des monobactames, qui appartiennent à la famille des beta-lactamines. Cette classe d’antibiotiques est active contre les bactéries à gram négatif. L’aztréonam est obtenu par synthèse totale. Les avantages de cette molécule sont une distribution extravasculaire et tissulaire rapide et l’absence d’accidents d’entérites pseudomembraneuses par respect des flores fécales.
Forme commerciale : AZACTAM® 1g : flacon de poudre pour usage parentéral ; voie IV et IM. Laboratoire Sanofi Aventis. Composition : Aztréonam : 1g Excipient : L-arginine q.s.p. pH=5 après reconstitution avec de l’EPPI Médicament soumis à prescription hospitalière Liste I
Mécanisme d'action
L’aztréonam interfère avec la structure de la paroi des bactéries à gram négatif. La rupture de la paroi entraîne la lyse de la bactérie.
Indications thérapeutiques
L’Azactam® est utilisé dans : - les infections des voies urinaires hautes et basses - les infections sévères à bactéries gram négatif sensibles : infections broncho-pulmonaires, septicémies, infections de la peau et parties molles, infections intra-abdominales, infections gynéco-obstétricales [1]. L'utilisation d'un autre agent antibiotique de manière concomitante est souvent d'usage. On parle souvent d'association avec les aminoglycosides et la pipéracilline.
Compatibilité
L’Azactam® peut être dilué dans la plupart des solutions de perfusion en particulier chlorure de sodium 0,45 et 0,9 %, glucose 5 et 10 %, mannitol 5 et 10 %.
Caractéristiques physico-chimiques
Les spectres UV dans l’eau et le méthanol sont très différents (voir spectre UV de l’aztréonam 10 µg/ml dans la phase mobile en annexe). Les caractéristiques UV de l’aztréonam sont pH dépendantes. Un point isobestique est présent à 250 nm.
- pKa
Les valeurs de pKa des groupements sulfonyle, amine et carboxyle sont respectivement -0,7 ; 2,75 et 3,91. A pH compris entre 0 et 10, l’aztréonam peut exister sous forme zwitterion, monoanion ou dianion.
La solubilité du zwitterion de l’aztréonam est limitée à pH 1-3 mais avec l’ionisation de la fonction carboxyle, elle augmente à pH supérieur à 3.
Stabilité
Les deux produits de dégradation principaux sont l’isomère E et le produit de dégradation provenant de l’ouverture du noyau bêta-lactame. Les autres produits de dégradation décrits sont la forme désulfonée et des oligomères.
La réaction d’isomérisation Z-aztréonam = E-aztréonam est la plus importante. Cette réaction est 100 fois plus importante que la réaction parallèle Z-aztréonam → produits, celle-ci étant elle-même 4 fois plus importante que la réaction E-aztréonam → produits[2].
L’aztréonam est utilisé à une concentration de 5 mg/l et 20 mg/l. La formulation inclut du glucose 5% ou du chlorure de sodium 0,9 %. L’aztréonam à une concentration de 10 mg/l et 20 mg/l dans du NaCl 0,9% est stable pendant 48 heures à 25 °C et pendant 7 jours à 4 °C[3]. Le temps nécessaire pour atteindre 10% de décomposition d’une solution d’aztréonam à 20g/ml dans du NaCl 0,9% conservée à 4 °C est 267 jours[4]. L’aztréonam à 10mg/l dans du NaCl 0,9% est stable jusqu’à 30 heures à température ambiante et 94 heures au réfrigérateur[5]. Une étude de stabilité de solutions d’aztréonam (5 mg/l et 20 mg/l) dans du glucose 5% et du chlorure de sodium 0,9 % dans des diffuseurs en polyisoprène valide une durée de 24 heures à 37 °C et de 8 jours au réfrigérateur[6]. Une autre étude rapporte une stabilité de 48 heures à température ambiante dans des seringues en polypropylène[7].
Effets secondaires
- Troubles gastro-intestinaux : nausées, vomissements, diarrhée
- Irritation au site d'injection
- Rash
- Fièvre
- Troubles hémodynamiques : leucopénie, neutropénie, éosinophilie
- Élévation des enzymes hépatiques
Allergies
Il n'y a aucune allergie croisée avec les autres β-lactames. (pénicillines, céphalosporines, ...)
Notes et références
- ↑ http://hoptimal.chu-nancy.fr, Vidal en ligne, consulté le 28/01/08
- ↑ ZAJAC M., JELINSKA A., CIELECKA-PIONTEK J., BAKLER, Stability of Aztreonam in AZACTAM, Il Farmaco 60 2005, 569-603
- ↑ JAMES M., RILEY C., Stability of intraveinous admixtures of aztreonam and ampicilline, Am J Hosp Pharm 1985, 42: 1095-1100
- ↑ MACLAUGHLIN J., SIMPSON C., The stability of reconstituted aztreonam, Practice research 1990 n° 1233, 328-334
- ↑ BELLIVEAU P., NIGHTINGALE C., QUINTILLIANI R., Stability of aztreonam and ampicilline sodium-sulbactam sodium in 0,9% sodium chloride injection, Am J Hosp Pharm 1994, 51 : 90 1-4
- ↑ VINKS A., TOUW D., VAN ROSSEN R., HEIJERMAN H., BAKKER W., Stability of aztreonam in a portable pump reservoir used for home intravenous antibiotic treatment, Pharm world sci 1996, 18 (2), 74-77
- ↑ MARBLE D.A., BOSSO J.A., TOWNSEND R.J., Compatibility of clindamycine phosphate with aztreonam in polypropylene syringues and with cefoperazone sodium, cefonicid sodium, and cefuroxine sodium in partial-fill glass bottles, Drug intelligence and clinical pharmacy 1988, 22 (1), 54-7
- Portail de la chimie
- Portail de la médecine
- Portail de la pharmacie
Catégorie : Antibiotique bêta-lactamine
Wikimedia Foundation. 2010.
