- 7783-41-7
-
Difluorure d'oxygène
Difluorure d'oxygène 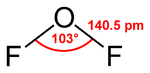
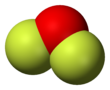
Structure du difluorure d'oxygèneGénéral Synonymes Fluorure d'oxygène
Monoxyde de fluor
Monoxyde de difluorNo CAS No EINECS Apparence gaz comprimé incolore, d'odeur caractéristique, jaunâtre à brun à l'état liquide.[1] Propriétés chimiques Formule brute OF2 Masse molaire 53,9962 g∙mol-1
F 70,37 %, O 29,63 %,Propriétés physiques T° fusion -224 °C[1] T° ébullition -145 °C[1] Solubilité dans l'eau à 0 °C : (réaction lente) 6.8 ml/100 ml[1] Masse volumique 1 900 kg/m3
liquide à -145 °CPrécautions Transport - 2190 SIMDUT[2] 



Unités du SI & CNTP, sauf indication contraire. Le difluorure d'oxygène, ou plus simplement fluorure d'oxygène, est le composé chimique de formule OF2. C'est un gaz incolore très oxydant.
Préparation
Le difluorure d'oxygène OF2 a été décrit pour la première fois en 1929 par le chimiste français Paul Lebeau au cours de ses recherches sur le fluor avec Augustin Damien. Il était obtenu par électrolyse de fluorure de potassium KF fondu et de fluorure d'hydrogène HF avec des traces de molécules d'eau.
La méthode de préparation moderne fait intervenir la réaction de fluor F2 avec une solution aqueuse diluée d'hydroxyde de sodium NaOH :
Réactions
Le difluorure d'oxygène se décompose au-dessus de 200 °C en fluor F2 et oxygène O2 par un mécanisme radicalaire. Il réagit avec de nombreux métaux pour donner des fluorures et des oxydes, ainsi qu'avec des non-métaux : OF2 réagit par exemple avec le phosphore pour donner le pentafluorure de phosphore PF5 et l'oxytrifluorure de phosphore POF3, et avec le soufre pour donner le dioxyde de soufre SO2 et le tétrafluorure de soufre SF4. Avec le xénon, OF2 peut donner du tétrafluorure de xénon XeF4 ainsi que des oxyfluorures de xénon (oxydifluorure de xénon XeOF2 et oxytétrafluorure de xénon XeOF4 notamment).
Le difluorure d'oxygène réagit lentement avec l'eau pour donner de l'acide fluorhydrique :
Notes et références
- ↑ a , b , c et d DIFLUORURE D'OXYGENE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ « Difluorure d'oxygène » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Portail de la chimie
Catégories : Composé du fluor | Produit chimique comburant | Produit chimique corrosif | Fluorure | Gaz inorganique | Composé de l'oxygène
Wikimedia Foundation. 2010.
