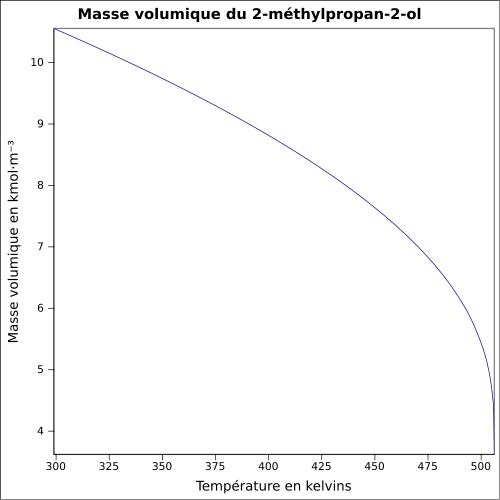
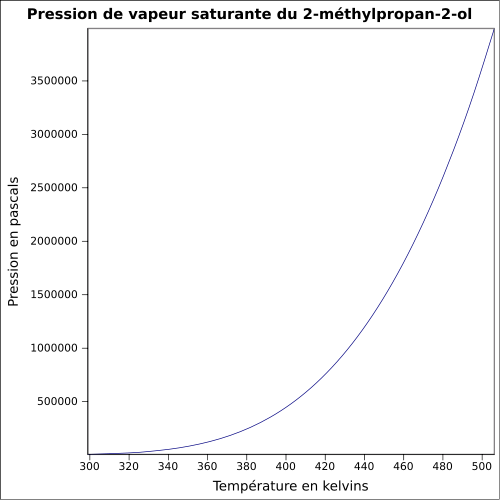
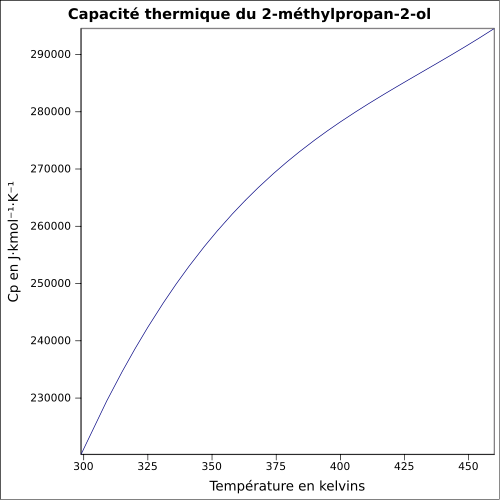
- 2-méthylpropan-2-ol
-
2-méthylpropan-2-ol 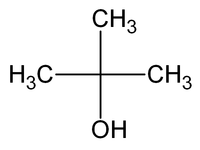
structure du 2-méthylpropan-2-ol Général Nom IUPAC 2-méthylpropan-2-ol Synonymes tert-butanol
Alcool tert-butylique.
TriméthylcarbinolNo CAS No EINECS Apparence liquide incolore ou poudre cristalline, d'odeur caractéristique[1]. Propriétés chimiques Formule brute C4H10O [Isomères] Masse molaire[3] 74,1216 ± 0,0042 g·mol-1
C 64,82 %, H 13,6 %, O 21,59 %,Moment dipolaire 1,66 D [2] Propriétés physiques T° fusion 25 °C[1] T° ébullition 83 °C[1] Solubilité dans l'eau : très bonne[1],
Complète dans les solvants polaires et apolaires (acétone, éther).Masse volumique 0,8 g·cm-3[1] T° d'auto-inflammation 470 °C[1] Point d’éclair 11 °C (coupelle fermée)[1] Limites d’explosivité dans l’air 2,4–8,0 %vol[1] Pression de vapeur saturante à 20 °C : 4,1 kPa[1] Viscosité dynamique 3,35 mPa*s (30 °C) Point critique 39,7 bar, 233,05 °C [5] Thermochimie Cp Propriétés électroniques 1re énergie d'ionisation 9,90 ± 0,02 eV (gaz)[7] Propriétés optiques Indice de réfraction  1,3852 [2]
1,3852 [2]Précautions Directive 67/548/EEC 
Xn
FPhrases R : 11, 20, Phrases S : (2), 9, 16, Transport - 1120 NFPA 704 SIMDUT[8] 

SGH[9] 

DangerInhalation Ébriété, nausée, vomissements Peau Irritation Yeux Irritation, irritation des muqueuses Ingestion Malaise, vomissements Écotoxicologie LogP 0,4[1] Seuil de l’odorat bas : 3,3 ppm
haut : 957 ppm[10]Unités du SI & CNTP, sauf indication contraire. Le 2-méthylpropan-2-ol, méthylpropan-2-ol, ou tert-butanol, est un alcool tertiaire de formule brute C4H10O. C'est un des isomères du butanol. À température supérieure à 24,3 °C, c'est un liquide transparent soluble dans l'eau, l'éthanol et l'éther
Sommaire
Utilisation
Le 2-méthylpropan-2-ol est utilisé comme solvant, dans les dissolvants pour peintures, dans le carburant pour augmenter l'indice d'octane, et comme intermédiaire dans la synthèse d'autres produits chimiques communs comme les parfums.
Propriétés physico-chimiques
L'encombrement stérique du groupe tert-butyle rend le tert-butanol beaucoup moins nucléophile que les autres isomères du butanol. En outre, il n'est pas oxydable en cétone puisque le carbone central est quaternaire.
En présence d'une base forte, le tert-butanol perd un proton et devient un ion alcoolate. Par exemple, la déprotonation par l'hydrure de sodium :
- NaH + tBuOH → tBuO- + Na+ + H2
Production et synthèse
Le 2-méthylpropan-2-ol peut être synthétisé industriellement par l'hydratation catalysée de l'isobutène.
Risques principaux
F : Inflammable Xn : Nocif
R11,R20,S2,S9,S16.
Voir aussi
Articles connexes
Références
- tert - BUTANOL, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, England, John Wiley & Sons Ltd, 1999, 239 p. (ISBN 0-471-98369-1)
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, 1997, 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50
- Properties of Various Gases sur flexwareinc.com. Consulté le 12 avril 2010
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 1, Huston, Texas, Gulf Pub. Co. (ISBN 0-88415-857-8)
- (en) David R. Lide, Handbook of chemistry and physics, CRC, 2008, 89e éd., 2736 p. (ISBN 978-1-4200-6679-1), p. 10-205
- « Alcool butylique tertiaire » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- tert-Butyl alcohol sur hazmap.nlm.nih.gov. Consulté le 14 novembre 2009
Catégories :- Produit chimique nocif
- Produit chimique facilement inflammable
- Alcool (chimie)
Wikimedia Foundation. 2010.