- Trinitrotoluene
-
Trinitrotoluène
 Pour les articles homonymes, voir TNT.
Pour les articles homonymes, voir TNT.Trinitrotoluène 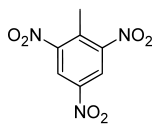
structure du Trinitrotoluène Général Nom IUPAC 1-methyl-2,4,6-trinitrobenzene No CAS No EINECS Apparence cristaux incolores à jaunes.[1] Propriétés chimiques Formule brute C7H5N3O6 [Isomères] Masse molaire 227,1311 g∙mol-1
C 37,02 %, H 2,22 %, N 18,5 %, O 42,26 %,Propriétés physiques T° fusion 80,1 °C[1] T° ébullition (décomposition) : 240 °C[1] Solubilité dans l'eau à 20 °C : 0.019 g/100 ml[1],
bonne dans l'éther, l'acétone, le benzèneMasse volumique (eau = 1) : 1.65[1] Pression de vapeur saturante 0.057 hPa (81 °C) Précautions Directive 67/548/EEC 
T
E
NPhrases R : 2, 23/24/25, 33, 51/53, Phrases S : 1/2, 35, 45, 61, [2] Transport - 0209
40 1356 SIMDUT[4] 

SGH[5] 



DangerClassification du CIRC Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[3] Écotoxicologie LogP 1.60[1] Unités du SI & CNTP, sauf indication contraire. Le trinitrotoluène (TNT) est un explosif, utilisé dans plusieurs mélanges, notamment en proportion égale avec le nitrate d'ammonium pour former l’amatol.
Sommaire
Historique
Le TNT a été découvert en 1863 par le chimiste allemand Joseph Wilbrand. Son potentiel explosif n'a pu être observé que plusieurs années plus tard, en raison de la difficulté à mettre au point un détonateur efficace vu son peu de sensibilité et parce qu'il était moins puissant que d'autres explosifs.
Cependant, il a plusieurs propriétés qui lui permettent d'être intégré au sein des torpilles et ainsi d'avoir un pouvoir destructeur plus important que les autres explosifs alors utilisés, comme l'acide picrique. L'armée allemande l'adopta en 1902, tandis que les Britanniques l'ont progressivement intégré à leur arsenal à partir de 1907.
C'est ainsi que, durant la Première Guerre mondiale, le pouvoir destructeur des torpilles de la marine militaire allemande était plus important que celui des britanniques car elles explosaient après avoir perforé la coque, tandis que les torpilles britanniques explosaient à son contact et donc dissipaient à l'extérieur du bateau une partie de l'énergie dégagée par l'explosion.
Chimie
Le TNT est un composé chimique de type hydrocarbure aromatique cristallin.
Il est préparé par nitration du toluène (C6H5CH3). Toute la difficulté de sa synthèse vient du fait que la température nécessaire à son obtention est proche de la température d'explosion du composé binitré (dinitrotoluène) formé intermédiairement.
Explosif
Sous sa forme raffinée, le trinitrotoluène est relativement stable et moins sensible que la nitroglycérine aux chocs et au transport. Son action explosive doit être amorcée par un détonateur. Il n'intéragit pas avec les métaux et n'absorbe pas l'eau, ce qui lui assure une stabilité pour des stockages assez longs, contrairement à la dynamite, mais il peut former des composés instables au contact de métaux alcalins.
L'énergie spécifique de combustion du TNT est de 4,6 mégajoule/kg, soit 1 kilotonne TNT = 4,6 TJ (térajoule), 1 mégatonne de TNT = 4,6 PJ (pétajoule). Cependant, par convention, quand on mesure l’énergie dégagée lors d’une explosion, on utilise le facteur de conversion 1 kg de TNT = 106 calories = 4,6 MJ.
On peut remarquer que les explosifs (non-nucléaires) produisent moins d’énergie par kilogramme que des produits alimentaires comme les matières grasses (38 mégajoule/kg) ou le sucre (17 mégajoule/kg). On peut noter trois différences essentielles entre ces chiffres :
- Les énergies spécifiques de combustion des combustibles ordinaires sont calculées sans tenir compte de la masse d'oxygène nécessaire à la combustion : si l'on en tient compte, il faut diviser le chiffre par plus de quatre pour les matières grasses, et environ deux pour les sucres ;
- La combustion des explosifs nitrés se faisant sans apport d'oxygène atmosphérique, elle est loin d'être complète : la quantité d'oxygène disponible n'est pour le TNT qu'un tiers environ de ce qui serait nécessaire pour une combustion complète ;
- Cependant, les explosifs ont des effets bien plus destructeurs, car ils libèrent leur énergie presque instantanément, n'ayant pas besoin d’oxygène externe pour leur combustion.
Unité de puissance explosive
La puissance des bombes, en particulier des bombes atomiques, est souvent désignée par un équivalent en TNT. On utilise alors la « kilotonne » (1 000 tonnes de TNT) ou la « mégatonne » (1 000 000 tonnes de TNT).
La bombe larguée sur Hiroshima en 1945 avait par exemple une puissance d'environ 15 kilotonnes, soit 15 000 tonnes de TNT (un cube de TNT de 21 mètres de côté). La bombe H la plus puissante jamais testée (record détenu par l'Union soviétique avec la Tsar Bomba, ou la Reine des bombes) était équivalente à 50 mégatonnes, 50 millions de tonnes de TNT (ou un cube de TNT d'à peu près 315 mètres de côté).
Toxicité
Beaucoup de terrains militaires sont contaminés par le TNT. Une exposition à de fortes doses peut provoquer des anémies et des maladies du foie. On a également observé des hypertrophies de la rate et des effets négatifs pour le système immunitaire chez des animaux qui avaient ingéré et respiré du trinitrotoluène, ainsi que des irritations cutanées. Les autres effets délétères sont une baisse de la fertilité masculine et un risque cancérigène (c'est un hydrocarbure aromatique, dont beaucoup de propriétés sont communes avec le benzène, de nature cancérigène). La consommation de TNT noircit l’urine.
Voir aussi
Articles connexes
- Toluène, benzène avec un groupement méthyle
- Nitrotoluène , toluène substitué par un groupement nitro
- Dinitrotoluène, toluène substitué par deux groupements nitro
- Dynamite
- Liste de composés explosifs
Notes et références
- ↑ a , b , c , d , e et f 2, 4, 6 - TRINITROTOLUENE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ « 2,4,6-trinitrotoluène » sur ESIS, consulté le 20 février 2009
- ↑ IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme » sur http://monographs.iarc.fr, 16 janvier 2009, CIRC. Consulté le 22 août 2009
- ↑ « Trinitro-2,4,6 toluène » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- Portail de la chimie
Catégories : Produit chimique toxique | Produit chimique explosif | Produit chimique dangereux pour l'environnement | Nitrobenzène | Méthylbenzène | Explosif
Wikimedia Foundation. 2010.


