- Na2SO4
-
Sulfate de sodium
Sulfate de sodium 
Général No CAS No EINECS No E E514 Apparence solide blanc Propriétés chimiques Formule brute Na2SO4
Heptahydrate Na2SO4·7H2O
Décahydrate: Na2SO4·10H2OMasse molaire 142,042 g∙mol-1
Na 32,37 %, O 45,06 %, S 22,58 %,Propriétés physiques T° fusion 884 °C, anhydre
32,4 °C décahydrateSolubilité 4.76 g dans 100 g d'eau (0 °C)
42.7 g dans 100 g d'eau (100 °C)Masse volumique 2.68 (anhydre) Thermochimie ΔfH0solide 78.2 kJ/mol Cristallographie Système cristallin monoclinique, orthorhombique ou hexagonal Précautions SIMDUT[1] Produit non contrôlé Peau Irritant Unités du SI & CNTP, sauf indication contraire. Le sulfate de sodium est un composé chimique courant formé d'un ion sulfate et de deux ions sodium. Lorsqu'il est anhydre, il prend l'apparence d'un solide cristallin blanc de formule chimique Na2SO4. La forme déca-hydratée, Na2SO4·10H2O, est connue sous le nom de sel de Glauber ou mirabilite. Parmi un grand nombre d'usages différents, les principales utilisations du sulfate de sodium concernent la fabrication des détergents et dans le procédé de Kraft de traitement de la pâte à papier. La moitié environ de la production mondiale provient de l'extraction de la forme naturelle décahydratée, et l'autre moitié de productions secondaires dans des procédés de l'industrie chimique.
Sommaire
Histoire
La forme naturelle décahydratée du sulfate de sodium porte le nom de sel de Glauber, ou sal mirabilis. Elle a été baptisée d'après Johann Rudolf Glauber, qui la découvrit au XVIIe siècle. Elle se présentait sous la forme de cristaux blancs ou transparents, utilisés originellement comme laxatifs.
Propriétés physiques et chimiques
Le sulfate de sodium est très stable chimiquement. Il ne se décompose pas même sous l'effet de la chaleur, et il ne réagit pas aux températures courantes avec des agents oxydants ou réducteurs. A des températures élevées, il peut être réduit en sulfure de sodium. Etant dérivé d'un acide fort (acide sulfurique H2SO4) et d'une base forte (soude NaOH), c'est un sel neutre dont la solution aqueuse est de pH 7.
Le sulfate de sodium peut réagir en solution aqueuse. Il réagit notamment avec une quantité équivalente d'acide sulfurique pour former un sel d'acide selon un équilibre chimique, comme par exemple dans la réaction suivante :
Na2SO4(aq) + H2SO4(aq) ⇔ 2 NaHSO4(aq)
En réalité, l'équilibre est beaucoup plus complexe et dépend à la fois de la concentration et de la température, tout en mettant en jeu d'autres sels d'acide.
Na2SO4 constitue typiquement un sulfate ionique. Il peut former des précipités en solution aqueuse lorsqu'il est combiné avec des sels de baryum ou de plomb qui forment des sulfates insolubles :
Na2SO4(aq) + BaCl2(aq) → 2 NaCl(aq) + (s)
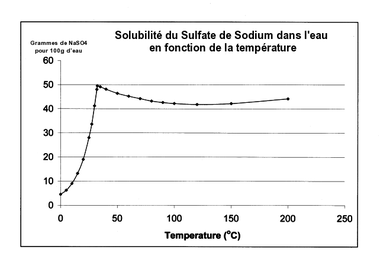
L'évolution de la solubilité du sulfate de sodium dans l'eau en fonction de la température est assez inhabituelle, comme le montre la courbe ci-après. La solubilité croît de plus d'un facteur 10 entre 0 °C et 32,4 °C, température à laquelle elle atteint un maximum de 49.7g pour 100g d'eau. A cette température, l'évolution change brusquement et la solubilité devient presque indépendante de la température. La solubilité est nettement plus faible si l'on ajoute du chlorure de sodium dans la solution. Cette évolution inhabituelle de la solubilité avec la température est à la base de l'utilisation du sulfate de sodium dans des systèmes passifs de chauffage solaire.
Cette caractéristique de la solubilité du sulfate de sodium peut être expliquée par le fait que 32,4 °C correspond à la température à laquelle la forme décahydratée ( sel de Glauber ) se décompose pour former une phase liquide est une phase solide anhydre.Extraction du sulfate de sodium
La moitié environ de la production mondiale provient de l'extraction de la forme décahydratée (sel de Glauber) du lit de lacs. En 1990, les principaux producteurs de sulfate de sodium naturel étaient le Mexique et l'Espagne (avec chacun environ 500 000 tonnes) suivis par l'URSS, les É.-U. et le Canada (avec chacun environ 350 000 tonnes).
On peut également trouver le sulfate de sodium dans une forme moins hydratée, la thenardite dans des environnements arides. Elle se transforme rapidement en mirabilite à l'air humide.
Production industrielle
La seconde moitié de la production mondiale est issue de productions secondaires de procédés de l'industrie chimique. La plus importante survient lors de la production d'acide chlorhydrique à partir de chlorure de sodium et d'acide sulfurique selon le procédé Mannheim. Le sulfate de sodium est alors appelé "gâteau de sel".
2 NaCl + H2SO4 → Na2SO4 + 2 HCl
Il est produit également à partir de dioxyde de soufre selon le procédé Hargreaves :
4 NaCl + 2 SO2 + O2 + H2O → 2 Na2SO4 + 4 HCl
Aux É.-U. et au Royaume-Uni, l'une des principales source de sulfate de sodium synthétique provient de la production de dichromate de sodium. Il y a également un grand nombre de procédés industriels au cours desquels un excès d'acide sulfurique est neutralisé par de la soude, ce qui conduit à la production de sulfate de sodium. Cette méthode est également la technique de fabrication la plus aisée en laboratoire :
2 NaOH(aq) + H2SO4(aq) → Na2SO4(aq) + 2 H2O(l)
Le sulfate de sodium est généralement purifié via la forme décahydratée, la forme anhydre ayant tendance à réagir avec les composés à base de fer et avec les composés organiques. La forme anhydre est ensuite produite par chauffage modéré de la forme hydratée.
Utilisation
En 1995, le sulfate de sodium se vendait environ 70$ la tonne aux États-Unis, ce qui en fait un composé chimique relativement bon marché. La première utilisation du sulfate de sodium à l'heure actuelle est probablement dans le domaine des détergents. La consommation totale en Europe était d'environ 1,6 million de tonnes en 2001, dont 80% dans le domaine des détergents. Cependant, cet usage tend à diminuer avec l'utilisation croissante de détergents sous forme liquide qui ne contiennent pas de sulfate de sodium.
Une des autres applications majeures du sulfate de sodium, tout particulièrement aux États-Unis, est dans le procédé Kraft de traitement de la pâte à papier. Les composés organiques présents dans la "liqueur noire" formée au cours de ce procédé sont brûlés pour produire de la chaleur, avec en parallèle une réduction du sulfate de sodium en sulfure de sodium. Cependant, ce procédé a été remplacé dans une certaine mesure par un nouveau procédé, et l'utilisation du sulfate de sodium dans l'industrie papetière américaine a décru de 980 000 tonnes en 1970 à 210 000 tonnes en 1990[réf. nécessaire].
L'industrie du verre est également une grande utilisatrice de sulfate de sodium, avec une consommation d'environ 30 000 tonnes en 1990 aux États-Unis (4% de la consommation totale). Il est utilisé pour réduire la quantité de petites bulles d'air dans le verre fondu. Il contribue également à fluidifier le verre, et à prévenir la formation de mousse dans le verre fondu durant l'élaboration.
Le sulfate de sodium est utilisé dans l'industrie textile, en particulier au Japon. Il réduit la quantité de charges négatives sur les fibres ce qui facilite la pénétration des teintures. Contrairement au chlorure de sodium, il a l'avantage de ne pas corroder les instruments en acier inoxydable utilisé pour la teinture.
Le sel de Glauber, la forme décahydratée, était utilisé dans le passé comme laxatif. Elle a également été proposée pour stocker la chaleur dans des systèmes passifs de chauffage solaire. Cette utilisation profite de ses propriétés de solubilité inhabituelle, ainsi que de sa chaleur de cristallisation élevée (78.2 kJ/mol).
Les autres utilisations du sulfate de sodium incluent le dégivrage des vitres, le nettoyage des moquettes et la fabrication d'amidon. Il est utilisé comme additif dans l'alimentation du bétail (numéro E514). En laboratoire, le sulfate de sodium anhydre est utilisé comme agent de séchage pour les solutions organiques.
Précautions à prendre
Bien que le sulfate de sodium soit généralement considéré comme non-toxique, il convient de le manipuler avec précautions.En effet, étant corrosif et irritant, il convient de porter des gants et des lunettes de protection lorsqu'il est manipulé sous sa forme cristalline.
Références
- . Handbook of Chemistry and Physics, 71st edition, CRC Press, Ann Arbor, Michigan, 1990.
- . The Merck Index, 7th edition, Merck & Co, Rahway, New Jersey, États-Unis, 1960.
- . "W. F. Linke, A. Seidell, Solubilities of Inorganic and Metal Organic Compounds, 4th edition, Van Nostrand, 1965.
- . D. Butts, in Kirk-Othmer Encyclopedia of Chemical Technology, 4th edition, v22, p403-411 (1997).
- . H. Nechamkin, The Chemistry of the Elements, McGraw-Hill, New York, 1968.
- . Maria Telkes, Improvements in or relating to a device and a composition of matter for the storage of heat, British Patent No. GB694553 (1953).
- ↑ « Sulfate de sodium » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 23 avril 2009
- Portail de la chimie
Catégories : Composé du sodium | Sulfate | Régulateur alimentaire de pH
Wikimedia Foundation. 2010.