- Anémie falciforme
-
Drépanocytose
Drépanocytose CIM-10 : D57 La drépanocytose (du grec drepnos, faucille), également appelée hémoglobinose S, sicklémie, ou anémie à cellules falciformes, est une maladie héréditaire et est caractérisée par l'altération de l'hémoglobine, protéine assurant le transport de l'oxygène dans le sang.
La drépanocytose n’est pas une maladie très rare. Elle est particulièrement fréquente dans les populations pauvres[réf. nécessaire] d'origine africaine sub-saharienne, avec une nette prédominance en Afrique équatoriale (chaque année 300 000 enfants africains naissent atteints de cette anomalie génétique), mais elle existe également en Afrique du nord, en Grèce, en Turquie, en Arabie saoudite et en Inde. On estime que 50 millions d'individus en sont atteints dans le monde[1].
C'est la première maladie génétique en France[2], et probablement dans le monde[3].Sommaire
Historique
En 1940, James Herrick, médecin à Chicago, fait la première description médicale de la drépanocytose: il examine un étudiant noir âgé de 20 ans, hospitalisé pour toux et fièvre. Le sujet est faible, a des vertiges et souffre de maux de tête. Depuis un an, il ressent des palpitations et un essoufflement comme certains membres de sa famille. L’examen du sang montre que le malade est très anémique, le nombre de ses hématies n’atteignant que la moitié de la valeur normale. L’observation d’un frottis sanguin montre des hématies inhabituelles en forme de faucille ou feuille d'acanthe.
En 1949, James Neel[4] démontre que la transmission de cette maladie est mendélienne. La même année Linus Pauling montre qu'elle est due à une structure anormale de l'hémoglobine, caractérisée par une moindre solubilité. C'est ainsi la première fois qu'on découvre l'origine moléculaire d'une maladie génétique.
En 1956, le Britannique Vernon Ingram montre qu'elle est due à un remplacement d'un acide aminé dans l'hémoglobine anormale[5]. Cela a démontré pour la première fois que les gènes déterminaient la nature de chaque acide aminé dans une protéine.
En 1978, Tom Maniatis isole le gène de la bêta globine.
Pathogénie
Au niveau cellulaire
Les globules rouges de l'homozygote, qui ne contiennent pratiquement que de l'HbS, acquièrent ainsi la propriété de se polymériser lorsqu'ils sont désoxygénés. Ceci explique que la falciformation des hématies soit déclenchée par le manque d'oxygène dans le sang (hypoxie) :
- in vivo, dans le sang veineux et capillaire : d'où séquestration prolongée, formation de thromboses et hémolyse facile des globules rouges dans les fins capillaires où les drépanocytes ont du mal à se frayer un passage, étant donné leur forme allongée, ainsi que dans la rate où la lenteur de la circulation crée les conditions requises pour la formation des drépanocytes, qui y seront phagocytés par le SRE.
- in vitro, lors de l'examen du sang frais entre lame et lamelle, lorsqu'on aura ajouté un corps réducteur (métabisulfite).
Au niveau moléculaire
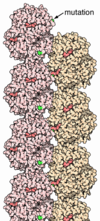
L'allèle S, est un allèle anormal du gène régissant la structure de la chaîne bêta de l'hémoglobine. Il est responsable de la synthèse de chaînes bêta, dont un des résidus d'acide glutamique en position 6 est remplacé par un résidu valine. L'hémoglobine qui en résulte appelée HbS (hémoglobine S pour Sickle-cell disease, dénomination anglaise de la maladie) a donc la structure "alpha2ß2S". Elle se distingue de l'hémoglobine A, normale, par sa mobilité électrophorétique plus lente, mais surtout par l'insolubilité de sa forme désoxygénée, qui cristallise facilement. Cela forme des fibres longues qui vont déformer le globule rouge.
Au niveau génétique
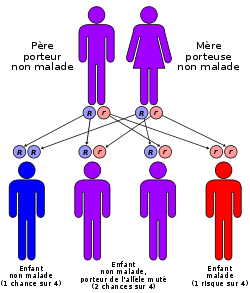
C'est le gène qui code la chaîne béta de l'hémoglobine qui est impliqué. Ce gène est porté par le chromosome 11. La version mutée (l'allèle S) de ce gène est responsable de l'anémie falciforme. C'est un allèle récessif : il faut que les deux copies de ce gène soient mutées pour que l'individu soit malade. Ainsi, un individu ne peut donc être atteint que si ses deux parents lui ont transmis l'allèle (S) responsable ; il est alors dit homozygote (S/S).
Chez l'hétérozygote (S/A), les globules rouges contiennent un mélange en proportions égales d'HbA et d'HbS. Lors de l'épreuve de désoxygénation entre lame et lamelle, ces globules rouges ne prennent pas la forme de faucilles, mais de feuilles de houx.
Au niveau de l'organisme
Les globules rouges ayant perdu leur élasticité vont obstruer les capillaires provoquant une ischémie par manque d'apport d'oxygène au niveau de différents territoires. Cela explique les crises douloureuses (infarctus osseux), les accidents vasculaires cérébraux. Les globules rouges pourraient également léser la paroi interne des vaisseaux (endothélium) entraînant un risque d'obstruction de ces derniers.
Ces globules rouges sont plus fragiles et vont se rompre beaucoup plus facilement, expliquant l'anémie de type hémolytique (par destruction hématies).
Épidémiologie
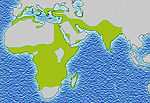 Distribution du paludisme
Distribution du paludisme
L'allèle S, responsable de l'anomalie, est surtout répandu dans le continent africain (atteignant dans certaines populations la fréquence de 30%); on le trouve également dans d'autres régions du bord de la Méditerranée, notamment en Italie (surtout en Sicile), en Grèce et en Anatolie.
Cette distribution se superpose assez bien avec celle d'une autre maladie, le paludisme ou malaria, qui, elle, a une origine infectieuse: le Plasmodium falciparum.
La présence élevée de cette maladie en Afrique semble être un cas de polymorphisme génétique équilibré entraîné par une sélection naturelle : en effet, les personnes porteuses saines hétérozygotes (A/S) ou atteintes de la drépanocytose homozygotes (S/S) sont protégées des affections neurologiques de Plasmodium, le parasite responsable du paludisme aussi appelé malaria. Au cours des générations, les individus porteurs sains de l'allèle S se sont donc mieux reproduit que les autres, ce qui a provoqué l'augmentation de la fréquence de cet allèle.
Symptômes
L'affection se signale chez le nourrisson, mais n'est d'ordinaire pas manifeste à la naissance parce que les globules rouges du nouveau-né contiennent encore 50-90% d'hémoglobine fœtale. Les symptômes de cette maladie peuvent apparaître dès l'âge de six mois. Les manifestations aiguës habituelles de la drépanocytose sont de trois ordres :
- Crises vaso-occlusives : des caillots bouchent une artère, ce qui entraîne des douleurs intenses et brutales dans une partie du corps (fréquemment mains, pieds, hanches, abdomen). Ces crises peuvent être très douloureuses.
- Anémie hémolytique : les globules rouges des drépanocytaires sont de forme anormale. Celles-ci prennent une forme de faucille, et sont arrêtées par le filtre que représente la rate, où elles sont détruites. Cette destruction entraîne une baisse du nombre d'hématies et donc une anémie régénérative.
- Infections : elles sont plus fréquentes chez les drépanocytaires, surtout à pneumocoques chez le jeune enfant[6]. Elles peuvent aussi aggraver l'anémie en cas d'infection par le parvovirus B19.
Les manifestations chroniques de la drépanocytose associent un retard de taille et de poids, des déficits nutritionnels (notamment en folates, car cette vitamine est indispensable à la création des hématies qui sont renouvelées très rapidement lors des crises d'anémie, épuisant ainsi le stock de folates), un retard pubertaire fréquent, des troubles cardio-pulmonaires (augmentation de la taille du cœur, insuffisance respiratoire), une rate augmentée de volume (mais qui avec le temps va régresser jusqu'à devenir de petite taille par atrophie), des anomalies rétiniennes (hémorragies), etc.
La destruction des hématies au niveau de la rate entraîne une occlusion des vaisseaux de cette dernière, en partie responsable de l'augmentation de la taille de celle-ci (splénomégalie). Au fil du temps, la rate ne peut plus remplir son rôle d'organe lymphoïde (on parle d'asplénie fonctionnelle), ce qui entraîne une sensibilité accrue à certains germes, notamment le méningocoque (Neisseria meningitidis) et le pneumocoque (Streptococcus pneumoniae).
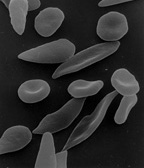 Hématies d'un drépanocytaire
Hématies d'un drépanocytaire
Image prise au microscope électronique du sang d'un patient hétérozygote pour la drépanocytose, sur laquelle on distingue des globules rouges sains, circulaires et concaves, des globules rouges malades possédant de l'hémoglobine mutée S, de la forme d'une faucille.
Examens et diagnostic
À part les constatations communes à toutes les anémies hémolytiques, le diagnostic repose sur la mise en évidence de l'hémoglobine S. Ceci peut se faire :
- par l'observation au microscope de sang frais conservé entre lame et lamelle, avec ou sans addition d'un réducteur (métabisulfite de potassium, acide ascorbique) : on verra les globules rouges de l'homozygote se transformer en faucilles et celles de l'hétérozygote en feuilles de houx (la cristallisation de l'hémoglobine S déforme la membrane),
- par l'électrophorèse de l'hémolysat de globules rouges qui montrera, chez l'homozygote, une bande unique d'une hémoglobine migrant anormalement lentement, et chez l'hétérozygote la présence de deux bandes d'hémoglobine, dont la plus rapide sera l'hémoglobine A et l'autre l'hémoglobine S.
- Aujourd'hui des tests permettent de dépister les porteurs sains (personnes hétérozygotes qui possèdent l'allèle responsable mais qui ne sont pas malades) ; ils sont alors informés que l'enfant conçu par deux porteurs sains présente un risque sur quatre d'être atteint d'anémie falciforme.
Dans les pays industrialisés, le diagnostic se fait en période néo-natale si les parents sont à risque ou atteints. Dans les pays non industrialisés, le diagnostic se fait souvent à la première manifestation ou complication. Le dépistage néo natal pourrait se traduire par une amélioration du pronostic[7].
Pronostic
La maladie peut se compliquer d'accidents vasculaires cérébraux dont la prévalence atteint près de 10% des patients âgés de moins de 20 ans[8]. L'hypertension artérielle pulmonaire est une complication fréquente (un tiers des cas) et grave[9].
Avant l'apparition de l'hydroxyurée près de la moitié des malades décédait avant l'âge de 50 ans, soit au cours d'une crise, ou d'un accident vasculaire cérébral[10].
Traitements
Le traitement de la drépanocytose repose sur :
- le traitement des crises vaso-occlusives : antalgiques (pouvant aller jusqu'aux opiacés) et mise sous oxygène ;
- la prévention des facteurs déclenchant les crises (froid, altitude, infections, déshydratation) ;
- la supplémentation en folates ;
- le traitement préventif des infections à pneumocoque et méningocoque ;
- la transfusion sanguine en cas d'anémie profonde ou d'infection grave.
L'hydroxyurée permet de favoriser la production d'hémoglobine fœtale, formée habituellement en petite quantité et parfaitement fonctionnelle, en inhibant la production d'hématies contenant l'hémoglobine S[11]. Ce médicament semble réduire significativement le nombre de crises douloureuses et la mortalité de la maladie[12]. Il ne peut cependant pas être utilisé, de par son mécanisme d'action, chez les patients anémiques. La surveillance des paramètres sanguins doit donc être très soigneuse. L'autre obstacle à son utilisation reste son coût, qui peut toutefois générer des économies de prise en charge dans les pays économiquement développés[13].
La prévention des infections par le pneumocoque chez le jeune enfant est faite par la vaccination[14].
Des transfusions sanguines pourraient diminuer sensiblement le risque d'accidents vasculaire-cérébraux chez certains enfants particulièrement à risque (anomalie du doppler trans-crânien)[15].
Mesures simples de prévention
Pour éviter les crises il est recommandé de suivre des mesures simples suivantes:
- boire fréquemment de l'eau
- bien aérer les pièces, afin de bien s'oxygéner
- rester au chaud
- ne pas prendre de poids
- manger des aliments riches en fer, ou qui facilitent l'assimilation du fer (viande rouge,pâté de foie ...)
- ne pas s'enrhumer, ou plus généralement éviter au maximum les infections respiratoires
- porter des vêtements qui ne coupent pas la circulation sanguine c'est à dire amples
- ne pas s'essouffler
- éviter d'aller à plus de 1500 mètres d'altitude
- ne pas s'exposer a de forte chaleur (la déshydratation déclenche des crises par augmentation de la viscosité sanguine [16]).
Greffe de moelle osseuse
Les hématies sont produites à partir de cellules souches dans la moelle osseuse. En détruisant la moelle osseuse du malade et en la remplaçant par celle d'un donneur, il y a possibilité d'obtenir une guérison totale. Environ 200 greffes ont été réalisées dans le monde chez des drépanocytaires, permettant d'obtenir la guérison dans 85 % des cas[17]. Il faut cependant un donneur apparenté le plus possible: un frère ou une sœur. Il y a la possibilité pour les parents de recourir à une fécondation in vitro avec sélection par DPI d'embryons compatibles pour la greffe. Cette voie de traitement dite du « bébé médicament » est très encadrée par les lois de bioéthique.
Article connexe : Transplantation de moelle.Voies de recherche
Des souris drépanocytaires ont pu être guéries en introduisant chez ces animaux un gène produisant une hémoglobine "anti-drépanocytaire" en quantité élevée[18].
Le 3 juin 2007, l'institut français de la propriété industrielle (INPI) a accordé à un médecin béninois, Jérôme Fagla Medegan, un brevet de découverte pour un médicament, le VK500, proposé dans le traitement de la drépanocytose[19]. Cependant, aucune étude clinique sérieuse n'a prouvé l'efficacité réelle de ce médicament dans la lutte contre la drépanocytose.
Liens externes
- (en) NCBI (NIH): Bibliographie sur Medline (en anglais) ;
- (fr) Orphanet: Informations sur la drépanocytose (consultations, recherches, associations...) (en français) ;
Références
- ↑ Arnal C. et Girot R. Drépanocytose chez l'adulte. Encycl Méd Chir (Éditions Scientifiques et Médicales Elsevier SAS, Paris), Hématologie, 13-006-D-16, 2002, 15p.
- ↑ Conférence de Canal U
- ↑ Association drepavie
- ↑ James Neel, The inhéritance of sickle cell anemia, Science vol.110, 1949, Page 543-548
- ↑ Ingram, V.M. (1956). "A Specific Chemical Difference between Globins of Normal and Sickle-cell Anemia Hemoglobins". Nature 178: 792-794.
- ↑ de Montalembert M, [http://www.bmj.com/cgi/content/extract/337/sep08_1/a1397 Management of sickle cell disease, BMJ, 2008;337:a1397
- ↑ Vichinsky E, Hurst D, Earles A, Kleman K, Lubin B, Newborn screening for sickle cell disease: effect on mortality, Pediatrics, 1998;81:749-54
- ↑ Balkaran B, Char G, Morris JS, Thomas PW, Serjeant BE, Serjeant GR, Stroke in a cohort of patients with homozygous sickle cell disease, J Pediatr,1992;120:360
- ↑ Gladwin MT, Sachdev V, Jison ML et als. Pulmonary hypertension as a risk factor for death in patients with sickle cell disease, N Engl J Med, 2004;350:886-95
- ↑ Platt OS, Brambilla DJ, Rosse WF, et als. Mortality in sickle cell disease: life expectancy and risk factors for early death, N Engl J Med, 1994;330:1639-1644
- ↑ Platt OS, Orkin SH, Dover G, Beardsley GP, Miller B, Nathan DG, Hydroxyurea enhances fetal hemoglobin production in sickle cell anemia, J Clin Invest, 1984;74:652-656
- ↑ Steinberg MH, Barton F, Castro O, et als. Effect of hydroxyurea on mortality and morbidity in adult sickle cell anemia: risks and benefits up to 9 years of treatment, JAMA, 2003;289:1645-1651
- ↑ Moore RD, Charache S, Terrin ML, Barton FB, Ballas SK, Cost-effectiveness of hydroxyurea in sickle cell anemia, Am J Hematol, 2000;64:26-31
- ↑ Davies EG, Riddington C, Lottenberg R, Dower N, Pneumococcal vaccines for sickle cell disease, Cochrane Database Syst Rev, 2004;(1):CD003885.pub2
- ↑ Adams RJ, McKie VC, Hsu L, Files B et als. Prevention of a first stroke by transfusions in children with sickle cell anemia and abnormal results on transcranial Doppler ultrasonography, N Engl J Med, 1998;339:5-11
- ↑ La prévention des crises sur le site de l'Association pour l'Information et la Prévention de la Drépanocytose
- ↑ Site des hôpitaux de Lyon, consulté le 30 avril 2008
- ↑ Pawliuk R, Westerman KA, Fabry ME et Als. [2001: Vol. 294. no. 5550, pp. 2368 - 2371 Correction of sickle cell disease in transgenic mouse models by gene therapy], Science, 2001:294;2368-2371
- ↑ Dépêche du journal Le Monde
- Portail de la médecine
Catégories : Maladie génétique en hématologie | Anémie | Pédiatrie
Wikimedia Foundation. 2010.