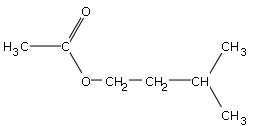
- Acétate d’isopentyle
-
Acétate d'isoamyle
Acétate d'isoamyle 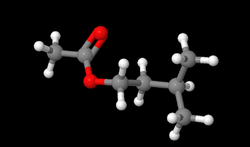
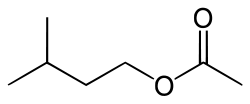
Modèle de Lewis Général Nom IUPAC Éthanoate d'isopentyle Synonymes Acétate d'isoamyle
Acétate d'isopentyle
Acétate de 3-méthylbutyleNo CAS No EINECS FEMA Apparence liquide incolore, d'odeur caractéristique.[1] Propriétés chimiques Formule brute C7H14O2 [Isomères] Masse molaire 130,1849 g∙mol-1
C 64,58 %, H 10,84 %, O 24,58 %,Propriétés physiques T° fusion -79 °C[1] T° ébullition 142 °C[1] Solubilité dans l'eau à 20 °C : 0.2 g/100 ml[1] Masse volumique (eau = 1) : 0.87[1] T° d’auto-inflammation 360 °C[1] Point d’éclair 25 °C c.f.[1] Limites d’explosivité dans l’air en volume % dans l'air : 1.0 (à 100 °C) -7.5[1] Pression de vapeur saturante à 20 °C : 0.53 kPa[1] Propriétés optiques Indice de réfraction 1,4003 Précautions Directive 67/548/EEC Phrases R : 10, 66, Phrases S : 23, 25, Transport - 1104 NFPA 704 SIMDUT[2] 
SGH[3] 
AttentionInhalation vapeur irritante Écotoxicologie LogP 2.13[1] Unités du SI & CNTP, sauf indication contraire. L'Acétate d'isoamyle ou acétate d'isopentyle est un ester, l'un des six isomères de l'acétate d'amyle.
Sommaire
Description
C'est un ester de l’acide acétique et de l'alcool isoamylique: C7H14O2 se présentant sous forme d'un liquide transparent, incolore, à odeur de banane ou encore d' "arlequin". Il est présent dans les pommes mûres. Il est utilisé dans la fabrication de peintures, ou comme agent de saveur. C'est aussi le phéromone d'alarme de l'abeille.
Propriétés physiques
- Densité de vapeur (air=1) : 4,49
- Tension de vapeur : 4 mm de Hg (0.53 kPa) à 20 °C
- Concentration à saturation : 5 000 ppm
- Coefficient de partage (eau/huile) : 0,0054
- Limite de détection olfactive : 0,025 ppm
- Facteur de conversion (ppm→mg/m³) : 5,325
- Taux d'évaporation (éther=1) : 12,2
Production par la levure
Dans la fermentation alcoolique d'un moût rosé ou lors de la macération carbonique il est possible d'obtenir une production naturelle d'acétate d'isoamyle qui participe aux caractéristiques de fraîcheur aromatique des vins ainsi obtenus : leurs arômes sont alors dit fermentaires.
Synthèse
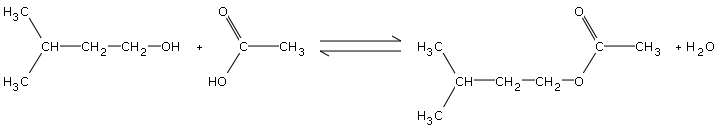
On peut en former par estérification de l'alcool isoamylique par l'acide éthanoïque :
La réaction est équilibrée, lente et athermique.
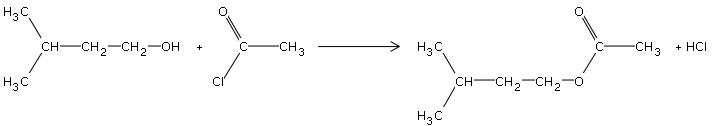
Il peut être aussi synthétisé avec le chlorure d'éthanoyle (→estérification à partir de dérivés d'acides carboxyliques) :
Par contre, ici, la réaction est totale, rapide et exothermique
Références
- Le parfum de la fraise, Peter Atkins (2005), Les éditions Dunod, ISBN 2-10-007596-9.
- ↑ a , b , c , d , e , f , g , h , i et j ACETATE D'ISOAMYLE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ « Acétate d'isoamyle » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
Ressources
- Portail de la chimie
- Portail de la vigne et du vin
Catégories : Vinification | Arôme | Acétate d'alkyle | Phéromone
Wikimedia Foundation. 2010.