- Acétanilide
-
Acétanilide 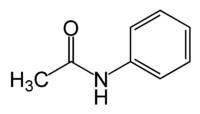
Général Nom IUPAC N-phényléthanamide Synonymes N-phénylacétamide
acétylaniline
acétylaminobenzèneNo CAS No EINECS PubChem ChEBI SMILES InChI Apparence cristaux blancs inodores Propriétés chimiques Formule brute C8H9NO [Isomères] Masse molaire[1] 135,1632 ± 0,0075 g·mol-1
C 71,09 %, H 6,71 %, N 10,36 %, O 11,84 %,Propriétés physiques T° fusion 114,3 °C [2] T° ébullition 304 °C [2] Masse volumique 1,2190 g·cm-3 à 15 °C [2] Thermochimie Cp Précautions Directive 67/548/EEC Phrases R : R 22 : nocif en cas d'ingestion[4] NFPA 704 SIMDUT[5] Produit non contrôlé Unités du SI & CNTP, sauf indication contraire. L'acétanilide, aussi appelé acétylaniline ou acétylaminobenzène, est une molécule organique de formule C8H9NO. C'est le précurseur de nombreuses drogues, colorants et autres composés dans la synthèse chimique. Autrefois utilisé comme analgésique et antipyrétique, il est souvent responsable de méthémoglobinémie mortelle. C'est un stabilisant du peroxyde d'hydrogène et des enduits cellulosiques. Il est utilisé dans la fabrication de produits pharmaceutiques comme le paracétamol. Il se présente sous la forme de cristaux blancs et brillants.
Sommaire
Propriétés physico-chimiques
L'acétanilide est soluble dans l'eau chaude. Ce composé, stable dans les conditions normales, devient autoinflammable lorsque la température atteint 545 °C. Il se présente sous forme de cristaux de couleur blanche lorsque le produit est pur.
Production et synthèse
On prépare l'acétanilide en faisant réagir l'anhydride acétique, soit avec l'aniline, soit avec le chlorure de phénylammonium.
Utilisation
Les domaines d'utilisation de l'acétanilide sont les suivants :
- inhibiteur pour le peroxyde d'hydrogène et stabilisateur des esters de cellulose.
- intermédiaire dans la synthèse du caoutchouc.
- synthèse du camphre.
- précurseur dans la synthèse de la pénicilline et autres produits pharmaceutiques.
- développement photographique (au XIXe siècle).
En outre, l’acétanilide a des propriétés analgésiques et réduit la fièvre. Elle se classe dans la même catégorie de médicaments que le paracétamol. Elle est souvent prescrite à de nombreux patients et on la trouve dans la plupart des pharmacies. En 1948, Julius Axelrod et Bernard Brodie ont découvert que l'acétanilide est beaucoup plus toxique dans ses utilisations que les autres médicaments, endommageant notamment le foie et les reins.
Références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- (en) W. M. Haynes, CRC Handbook of chemistry and physics, Boca Raton, CRC Press/Taylor and Francis, 2011, 91e éd., 2610 p. (ISBN 978-143982-077-3), p. 3-4
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 3, Huston, Texas, Gulf Pub. Co. (ISBN 0-88415-859-4)
- " title="Linkification: http://www.merck-chemicals.com/france/acetanilide/MDA_CHEM-100011/p_vdCb.s1LkWYAAAEW8OAfVhTl">http://www.merck-chemicals.com/france/acetanilide/MDA_CHEM-100011/p_vdCb.s1LkWYAAAEW8OAfVhTl
- « Acétanilide » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
Voir aussi
Liens externes
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « acetanilide » (voir la liste des auteurs)
Catégories :- Acétanilide
- Procédé photographique
Wikimedia Foundation. 2010.




