- Acide β-phénylacrylique
-
Acide cinnamique
Acide cinnamique 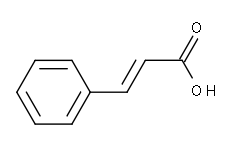
structure plane de l'acide cinnamique Général Nom IUPAC acide (E)-3-phényl-prop-2-ènoïque No CAS No EINECS FEMA Apparence cristal monoclinique blanc Propriétés chimiques Formule brute C9H8O2 [Isomères] Masse molaire 148,1586 g∙mol-1
C 72,96 %, H 5,44 %, O 21,6 %,pKa 4,44 Propriétés physiques T° fusion 135 à 136 °C (408-409 K) T° ébullition 300 °C Solubilité 0,4 g/L dans l'eau Masse volumique 1,2475 Point d’éclair >110 °C Thermochimie ΔfH0solide -325,3 kJ/mol Cp 197,5 J/mol·K (solide) Précautions SIMDUT[1] Produit non contrôlé Écotoxicologie DL50 2 500 mg/kg (oral, rat) Unités du SI & CNTP, sauf indication contraire. L'acide cinnamique de formule C6H5 - CHCHCOOH est un acide qui se présente sous la forme d'une poudre blanche inodore, avec une faible solubilité dans l'eau.
Il est obtenu à partir de l'extrait de cannelle, à laquelle son ester éthylique lui donne son odeur caractéristique, ou de certains arbustes balsamiques. Il peut aussi être synthétisé de novo. Il a été découvert et purifié par Péligot et Dumas en 1834. Il forme aussi une partie importante du baume de Tolu et du baume du Pérou. Ses esters sont présents dans le styrax.
Il est principalement utilisé dans l'industrie du parfum, où ses esters de méthyle, d'éthyle et de benzyle sont odorants et recherchés. Il sert aussi pour la composition d'exhausteurs de goût, d'indigo synthétique et de certains produits pharmaceutiques.
L'acide cinnamique est aussi un intermédiaire dans la voie de biosynthèse de l'acide shikimique, ainsi que de tous les phénylpropanoïdes.
Il possède par ailleurs des propriétés antiseptique et antifongique, connues dès la période précolombienne, ainsi qu'en témoigne le taux de guérison élevé des trépanations réalisées à l'époque (Voir l'article Médecine dans la préhistoire et la protohistoire). Il est encore utilisé à la même époque dans le processus de momification.
Sommaire
Synthèse au laboratoire
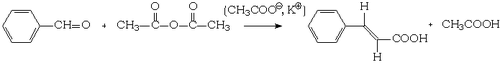
De nombreuses méthodes de synthèse de ce composé important ont été mises au point. La synthèse historique a été réalisé en 1856 par Cesare Bertagnini à partir de l'aldéhyde benzoïque et du chlorure d'acetyle.
On peut citer les deux suivantes :
Réaction de Perkin
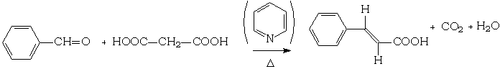
Réaction de Döbner-Knövenagel
Biosynthèse
L'acide cynnamique est biosynthétisé par une grande partie des végétaux. Il est produit par l'action de la phénylalanine ammonia-lyase (PAL) sur la phénylalanine.
Il sert alors d'intermédiaire à la synthèse d'autres phénylpropanoïdes.
Références
- Perkin, W. H.; J. Chem. Soc. 1868, 21, 53, 181.
- Perkin, W. H.; J. Chem. Soc. 1877, 31, 388.
- Réaction de Döbner-Knövenagel
- The Merck index : an encyclopedia of chemicals, drugs, and biologicals / Maryadele J. O'Neil, senior editor ; Ann Smith, senior associate editor ; Patricia E. Heckelman, associate editor, Whitehouse Station, New Jersey. : Merck, 2001.
- ↑ « Acide cinnamique » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
Liens externes
Source
- (en) Cet article est partiellement ou en totalité issu d’une traduction de l’article de Wikipédia en anglais intitulé « Cinnamic acid ».
- Portail de la chimie
Catégories : Acide cinnamique | Composé aromatique | Arôme
Wikimedia Foundation. 2010.