- Acide hippurique
-
Acide hippurique 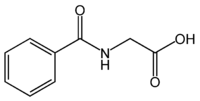
Général Nom IUPAC acide benzoylaminoacétique No CAS No EINECS Propriétés chimiques Formule brute C9H9NO3 [Isomères] Masse molaire[1] 179,1727 ± 0,0089 g·mol-1
C 60,33 %, H 5,06 %, N 7,82 %, O 26,79 %,Propriétés physiques T° fusion 187 à 188 °C T° ébullition 240 °C (décomposition) Précautions SIMDUT[2] Produit non contrôlé Unités du SI & CNTP, sauf indication contraire. L'acide hippurique est un dérivé des acides aminés constitué d'un acide benzoïque et de glycine. C'est une molécule qu'on trouve dans l'urine des chevaux (d'où son nom), ainsi que dans celle d'autres herbivores. C'est une molécule surtout connue pour les tests urinaires. En effet, l'acide paraamino-hippurique (PAH) est utilisé pour détecter des insuffisances rénales. C'est une substance exogène qui est filtrée et sécrétée. Sa clairance permet donc de déterminer s'il y a une insuffisance rénale glomérulaire et/ou tubulaire.
C'est un composant qui est trouvé en grande quantité dans les urines des herbivores. Chez l'homme il se forme après inhalation de toluène, qui sera métabolisé dans le foie et transformé en partie en acide benzoïque.
Sommaire
Histoire
Justus von Liebig a montré en 1829 que l'acide hippurique différait de l'acide benzoïque et en 1839 détermina sa constitution, alors qu'en 1873, Victor Dessaignes le synthétisa pour la première fois en faisant réagir du chlorure de benzoyle sur un sel de zinc de glycine[3]. Il a aussi été synthétisé plus tard en chauffant de l'anhydride benzoïque avec de la glycine[4], ou en chauffant du benzamide avec de l'acide chloroacétique.
Synthèse
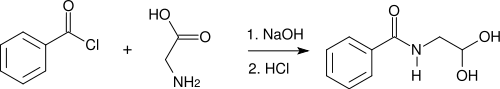
Outre les synthèses historiques citées plus haut, une méthode moderne de synthèse de l'acide hippurique est l'acylation de la glycine par le chlorure de benzoyle[5] :
Il s'agit d'un processus classique d'acylation; le carbone du groupe chlorure d'acyle, du fait de l'électronégativité de ses substituants et par la délocalisation possible de la double liaison C=O sur l'oxygène, est électrophile, et peut subir une substitution nucléophile de la part du groupe amine de la glycine, l'ion chlorure étant de plus un bon groupe partant.
Réactions
L'acide hippurique est facilement hydrolysé par une solution basique chaude en acide benzoïque et en glycine. L'action de l'acide nitreux le convertit en acide benzoylglycolique (C6H5C(=O)OCH2CO2H). Son ester éthylique réagit avec l'hydrazine pour former l'hydrazine hippuryle (C6H5CONHCH2CONHNH2), qui a été utilisée par Theodor Curtius pour la préparation de l'azoimide.
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- « Acide hippurique » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Dessaignes V., « Ueber die Regeneration der Hippursäure », dans Annalen der Chemie und Pharmacie, vol. 87, no 3, 1853, p. 325–327 [lien DOI]
- Curtius T., « Synthese von Hippursäure und Hippursäureäthern », dans Berichte der deutschen chemischen Gesellschaft, vol. 17, no 2, 1884, p. 1662–1663 [lien DOI]
- A. W. Ingersoll and S. H. Babcock. "Hippuric acid". Org. Synth.; Coll. Vol. 2: 0328.
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Hippuric acid » (voir la liste des auteurs)
Voir aussi
Wikimedia Foundation. 2010.