- 536-74-3
-
Phényléthyne
Phényléthyne 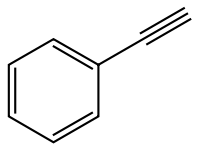
Général Nom IUPAC éthynylbenzène Synonymes phénylacétylène No CAS No EINECS PubChem SMILES InChI Apparence liquide incolore visqueux Propriétés chimiques Formule brute C8H6 [Isomères] Masse molaire 102,1332 g∙mol-1
C 94,08 %, H 5,92 %,Propriétés physiques T° fusion -44,8 °C [1] T° ébullition 415 à 417 °C [1] Solubilité 456 mg∙l-1 (eau,20 °C)[2] Masse volumique 0,9281 g∙ml-1 à 20 °C [3] Point d’éclair 31 °C [3] Thermochimie S0liquide, 1 bar 221,2 J∙mol-1∙K-1 [1] ΔfH0gaz 306,6 kJ∙mol-1 [1] ΔfH0liquide 284,3 kJ∙mol-1 [1] ΔfusH° 9,46 kJ∙mol-1 à -45,1 °C [1] Cp 180,1 J∙mol-1∙K-1 (liquide,25 °C)
150,41 J∙mol-1∙K-1 (gaz,126,9 °C)[1]PCI -4 289,9 kJ∙mol-1 [1] Précautions Directive 67/548/EEC 
F+NFPA 704[4] Écotoxicologie DL50 100 mg∙kg-1 (souris, intraveineuse) [2] LogP 2.53 [2] Unités du SI & CNTP, sauf indication contraire. Le phényléthyne ou phénylacétylène est un hydrocarbure alcynique contenant un groupe phényle. C'est un liquide incolore visqueux. En recherche, il est parfois utilisé comme un analogue de l'acétylène car, étant liquide, il est plus simpe à manipuler qu'un gaz comme l'acétylène.
Production et synthèse
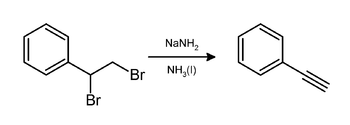
En laboratoire, le phényléthyne peut être préparé par élimination de bromure d'hydrogène (HBr) du dibromo-styrène en utilisant de l'amidure de sodium dans l'ammoniac[5] :
Il peut aussi être préparé de la même façon mais en utilisant de l'hydroxyde de potassium en fusion à 200 °C[6]
Caractéristiques physico-chimiques
- Le phényléthyl peut être réduit (hydrogéné) par l'hydrogène en styrène avec le catalyseur de Lindlar.
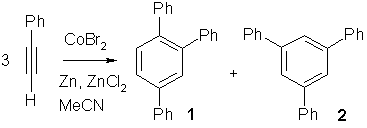
- Il subit une trimérisation catalysé par le cobalt pour former le 1,2,4- (97%) et le 1,3,5-triphénylbenzène[7]:
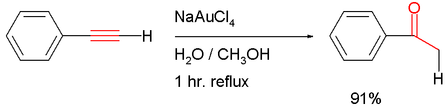
- Il subit une hydrolyse catalysée par l'or qui donne l'acétophénone.
Notes
- (en) Cet article est partiellement ou en totalité issu d’une traduction de l’article de Wikipédia en anglais intitulé « Phenylacetylene ».
- ↑ a , b , c , d , e , f , g et h (en) « Phenylacetylene » sur NIST/WebBook, consulté le 22 juillet 2009
- ↑ a , b et c (en) « Ethynylbenzene » sur ChemIDplus, consulté le 22 juillet 2009
- ↑ a et b « PHENYLACETYLENE » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 22 juillet 2009
- ↑ UCB Université du Colorado
- ↑ Phenylacetylene, Kenneth N. Campbell and Barbara K. Campbell, Org. Synth., 1963, vol. 4, p. 763.
- ↑ Phenylacetylene, John C. Hessler, Org. Synth., 1941, vol. 1, p. 438.
- ↑ A simple cobalt catalyst system for the efficient and regioselective cyclotrimerisation of alkynes, Gerhard Hilt , Thomas Vogler, Wilfried Hess, Fabrizio Galbiati; Chemical Communications, 2005, vol. 2005(11), pp. 1474–1475. DOI:10.1039/b417832g
- Portail de la chimie
Catégories : Produit chimique extrêmement inflammable | Alcyne | Composé aromatique
Wikimedia Foundation. 2010.