- Glycéraldéhyde-3-phosphate déshydrogénase
-
Glycéraldéhyde-3-phosphate déshydrogénase 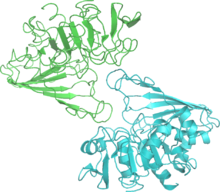
Unité asymétrique de 3GPD de muscle squelettique humain (voir 3GPD).N° EC EC N° CAS Bases de données IntEnz Vue IntEnz BRENDA Entrée BRENDA IUBMB 1.2.1.12 à l'IUBMB KEGG Entrée KEGG MetaCyc Voie métabolique PRIAM Profil PDB Structures GO AmiGO / EGO La glycéraldéhyde-3-phosphate déshydrogénase (abrégée en GAPDH ou, moins couramment, en G3PDH) est une enzyme qui catalyse la sixième étape de la glycolyse et donc intervient dans la dégradation du glucose afin de produire de l'énergie et du pouvoir réducteur sous forme respectivement d'ATP et de NADH + H+ destinés par la suite à produire les composés carbonés dont pourrait avoir besoin la cellule. Outre cette fonction métabolique essentielle, la GAPDH a plus récemment été impliquée dans plusieurs processus non métaboliques, tels que l'activation de la transcription, l'initiation de l'apoptose et le transfert de vésicules entre le réticulum endoplasmique et l'appareil de Golgi.
Sommaire
Fonction métabolique
La GAPDH catalyse la seule réaction d'oxydation de la glycolyse ; elle porte sur la fonction aldéhyde du glycéraldéhyde-3-phosphate (GAP) et produit un acyl-phosphate, le 1,3-diphosphoglycérate. La réaction d'oxydation est couplée au transfert d'un phosphate inorganique sur la molécule de GAP et à la réduction d'un NAD+ en NADH + H+.
La GAPDH catalyse également la réaction inverse lorsque la néoglucogénèse prédomine sur la glycolyse.
Réaction catalysée
La glycéraldéhyde-3-phosphate déshydrogénase catalyse, en présence de phosphate inorganique, la phosphorylation oxydative réversible du glycéraldéhyde-3-phosphate en 1,3-diphosphoglycérate en utilisant le nicotinamide adénine dinucléotide (NAD+) en tant qu'accepteur d'électrons.
- Glycéraldéhyde-3-phosphate + NAD+ + Pi = 1,3-diphosphoglycérate + NADH + H+
- Sens 1 : glycolyse.
- Sens 2 : néoglucogénèse.
Mécanisme catalytique
Le mécanisme catalytique de la GAPDH est constitué de deux étapes[1]:
- 1. Réaction d'oxydo-réduction
Après la liaison du glycéraldéhyde-3-phosphate (G3P) sur le site actif de l'enzyme, le groupement sulfhydryle (-SH) de la cystéine 149 du site catalytique réalise une attaque nucléophile de la fonction aldéhyde du G3P et forme un thiohémiacétal intermédiaire (catalyse covalente). Le thiohémiacétal subit alors une oxydation en acyl-thioester par le NAD+ lié à l'enzyme. L'énergie fournit par l'oxydation de la fonction aldéhyde permet en plus de la réduction d'un NAD+ en NADH, la synthèse d'un thioester intermédiaire, possédant une liaison à haut potentiel énergétique. Le transfert des deux électrons et du proton entre le G3P et la NAD+ est assisté par l'histidine 176 du site catalytique de l'enzyme.
- 2. Phosphorylation
Après remplacement du NADH formé par une nouvelle molécule de NAD+, l'acyl-thioester intermédiaire subit une attaque nucléophile par un phosphate inorganique. Un acide 1,3-diphosphoglycérique, un anhydride mixte à haut potentiel énergétique, est libéré et l'enzyme est régénérée.
Pour un schéma du mécanisme réactionnel de la GAPDH, de Molecular Cell Biology, Lodish, H, (200) 4th edition. W. H. Freeman.
La réaction catalysée par la GAPDH illustre comment l'énergie libérée dans une réaction d'oxydation est utilisée pour fabriquer un composé possédant une liaison à haut potentiel énergétique. Il s'agit d'un couplage énergétique par un mécanisme de transfert d'énergie entre une réaction d'oxydation exergonique et une réaction de phosphorylation d'un substrat endergonique. Dans l'étape suivante de la glycolyse (étape 7), l'énergie transférée dans l'acide 1,3-diphosphoglycérique sera utilisé pour fabriquer une molécule d'ATP.
Caractéristiques structurales
La GAPDH est un homotétramère dont les sous-unités ont une masse moléculaire variant de 34 à 38 kDa. Une sous-unité est composée d'environ 330 acides aminés qui se replient en formant deux domaines. Le premier domaine est impliqué dans la fixation du cofacteur (NAD+) : chacune des sous-unités fixe donc une molécule de NAD+. Le second domaine est impliqué dans la fixation du substrat et dans la catalyse : ce domaine contient la cystéine 149 et l'histidine 176, deux résidus essentiels au mécanisme catalytique.
Localisation cellulaire
L'ensemble des réactions de la glycolyse ayant lieu dans le cytosol, la GAPDH est une enzyme cytosolique. Des études de la membrane plasmique des globules rouges ont toutefois montré que certaines enzymes de la glycolyse, l'aldolase, la phosphofructokinase et la GAPDH, se lient de manière spécifique et réversible à la partie cytoplasmique de la protéine membranaire bande 3 (canal anionique).
Fonctions non métaboliques
Les autres classes de GAPDH
En plus de la GAPDH décrite précédemment, il existe deux autres classes de GAPDH qui se distinguent de la précédente par leur fonction enzymatique, leur localisation cellulaire et leur spécificité vis-à-vis du cofacteur, NAD ou NADP.
- GAPDH chloroplastiques (EC )[2], retrouvées spécifiquement dans les chloroplastes des organismes photosynthétiques où elles interviennent dans le cycle de Calvin. Cette classe de GAPDH possède une préférence pour le NADP+, cohérente avec son implication dans une voie anabolique. Les enzymes de cette classe catalysent la déphosphorylation réductrices du 1,3-DPG en G3P en parallèle avec l'oxydation d'une molécule de NADPH.
- GADPH non phosphorylantes (EC )[3], cytosoliques, qui catalysent l'oxydation irréversible du G3P en 3-phosphoglycérate (3PG) en présence de NADP+ et d'une molécule d'eau.
Notes et références
- S. Moniot et al. (2008), "Trapping of the thioacylglyceraldehyde-3-phosphate dehydrogenase intermediate from B.stearothermophilus." JBC. Vol.283, pp 21683-21702, August 1, 2008.
- G. Ferri et al. (1978), "Subunit structure and activity of glyceraldehyde-3-phosphate dehydrogenase from sinach chloroplasts." Biochem Biophys Acta. 522(1):19-31.
- Iglesias AA and Losada M. "Purification and kinetic and structural properties of spinach leef NADP-dependent nonphosphorylating glyceraldehyde-3-phosphate dehydrogenase." Arch Biochem Biophys. 260(2):830-40.
Références bibliographiques
- (fr) Biochimie générale, J.H. Weil (1990), sixième édition. Masson.
- (en) Molecular biology of the cell, B. Alberts & al. (2002), fourth edition. Garland Science.
- (en) Biochemistry, J.G. Voet, D. Voet (1995), second edition. John Wiley & sons, Inc.
Catégories :- EC 1.2.1
- Glycolyse
Wikimedia Foundation. 2010.
