- Fluoroacétate de sodium
-
Fluoroacétate de sodium 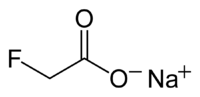
Général Nom IUPAC 2-fluoroacétate de sodium Synonymes 1080 No CAS No EINECS No RTECS PubChem ChEBI SMILES InChI Propriétés chimiques Formule brute C2H2FNaO2 [Isomères] Masse molaire[1] 100,0243 ± 0,0023 g·mol-1
C 24,02 %, H 2,02 %, F 18,99 %, Na 22,98 %, O 31,99 %,Précautions Directive 67/548/EEC[2] 
T+
NPhrases R : 26/27/28, 50, Phrases S : 13, 22, 36/37, 45, 61, Transport - 2629 Unités du SI & CNTP, sauf indication contraire. Le fluoroacétate de sodium, aussi connu sous son nom commercial, le 1080 (ce nom est son numéro dans le catalogue des poisons et est devenu son nom commercial[3]) est un composé organo-fluoré de formule FCH2CO2Na. C'est un sel incolore qui est utilisé comme poison métabolique. Il est naturellement présent dans de nombreuses plantes, jouant le rôle de métabolite anti-herbivore, mais est aussi synthétisé, notamment à partir de l'acide fluoroacétique.
Sommaire
Histoire
L'action rodenticide du fluoroacétate de sodium a été rapporté pour la première fois en 1942[4]. Il a depuis utilisé à cet usage, mais son utilisation a chuté depuis qu'il a été banni dans un certain nombre de pays.
Caractéristiques
Le fluoroacétate de sodium se présente sous la forme d'une poudre incolore et inodore, facilement soluble dans l'eau. Son point de fusion est de 200 °C.
Occurrence naturelle
Le fluoroacétate de sodium est naturellement présent dans au moins 40 plantes d'Australie, d'Amérique du Sud et d'Afrique. Il a été identifié la première fois dans la feuille toxique de Dichapetalum cymosum par Marais en 1944[5],[6]. Dès 1904, des colons au Sierra Leone ont utilisé des extraits de Chailletia toxicaria qui contient de l'acide fluoroacétique ou ses sels comme raticide[7],[8]. On pense que ce composé est également présent dans les feuille de thé, en très faible quantité[9]. En Australie, parmi les plantes contenant cette toxine on compte la famille de pois australiens Gastrolobium (« poison peas ») mais aussi des plantes de la famille Gompholobium, Oxylobium, Nemcia et Acacia. La présence de telles plantes dans leurs champs ont souvent forcé les fermiers de l'Australie occidentale à « scalper » leurs champs, c'est-à-dire de retirer la couche supérieure du sol et toutes les graines de poison peas qu'elle pourrait contenir, la remplacer par une nouvelle couche, vierge de poison, issue d'ailleurs, et d'y faire pousser leur semences.
Synthèse
Il est possible de synthétiser le fluoroacétate de sodium en faisant réagir le chloroacétate de sodium avec le fluorure de potassium[10] :
Il est également relativement simple de le synthétiser à partir de l'acide fluoroacétique, en faisant réagir ce dernier avec un sel de sodium comme l'hydroxyde de sodium :
le carbonate de calcium :
ou encore l'hydrogénocarbonate de sodium :
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- Sodium fluoroacetate chez Sigma-Aldrich.
- Proudfoot AT, Bradberry SM, Vale JA, « Sodium fluoroacetate poisoning », dans Toxicol Rev, vol. 25, no 4, 2006, p. 213–9 [lien PMID, lien DOI]
- Kalmbach ER, « Ten-Eighty, a War-Produced Rodenticide », dans Science, vol. 102, no 2644, 1945, p. 232–3 [lien PMID, lien DOI]
- Marais JCS, « The isolation of the toxic principle “K cymonate” from “Gifblaar”, Dichapetalum cymosum », dans Onderstepoort Jour. Vet. Sci. Animal Ind., vol. 18, 1943, p. 203
- Marais JCS, « Monofluoroacetic acid, the toxic principle of “gifblaar” Dichapetalum cymosum », dans Onderstepoort Jour. Vet. Sci. Animal Ind., vol. 20, 1944, p. 67
- Renner, « Chemical and Physiological Examination of the Fruit of Chailletia Toxicaria », dans Jour African Soc., 1904, p. 109
- Power FB, Tutin F, « C hemical and Physiological Examination of the Fruit of Chailletia Toxicaria », dans J. Am. Chem. Soc., vol. 28, 1906, p. 1170 [lien DOI]
- Vartiainen T, Kauranen P, « The determination of traces of fluoroacetic acid by extractive alkylation, pentafluorobenzylation and capillary gas chromatography-mass spectrometry », dans Anal Chim Acta, vol. 157, no 1, 1984, p. 91–7 [lien DOI]
- Jean Aigueperse, « Ullmann's Encyclopedia of Industrial Chemistry », Wiley-VCH, 2005 DOI:10.1002/14356007.a11_30
Catégories :- Composé du sodium
- Produit chimique très toxique
- Produit chimique dangereux pour l'environnement
- Composé organo-fluoré
- Rodenticide
- Inhibiteur d'enzyme
Wikimedia Foundation. 2010.







