- Cinnamate d'éthyle
-
Cinnamate d'éthyle 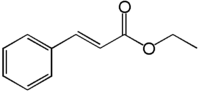
Général Nom IUPAC 3-phénylprop-2-énoate d'éthyle No CAS No EINECS No RTECS PubChem SMILES InChI Apparence liquide incolore Propriétés chimiques Formule brute C11H12O2 [Isomères] Masse molaire[1] 176,2118 ± 0,0102 g·mol-1
C 74,98 %, H 6,86 %, O 18,16 %,Propriétés physiques T° fusion 6 °C[2] T° ébullition 271 °C (1,013 bar)[2] Solubilité pratiquement insoluble dans l'eau[2] Masse volumique 1,05 g·cm-3 (20 °C[2] Point d’éclair > 110 °C (coupelle fermée)[2] Propriétés optiques Indice de réfraction  1,558[3]
1,558[3]Précautions Directive 67/548/EEC[2] Phrases S : 23, 24/25, Transport[2] non-soumis à régulation Écotoxicologie DL50 4 g·kg-1 (souris, oral)[4] LogP 2,99 [2] Unités du SI & CNTP, sauf indication contraire. Le cinnamate d'éthyle est l'ester de l'acide cinnamique et de l'éthanol. Il est naturellement présent dans l'huile essentielle de cannelle et dans la Kaempferia galanga[5],[6]
Principalement existant dans la nature sous forme trans ((E) cinammate d'éthyle), il se présente sous la forme d'un liquide incolore et sa forme pure a « une odeur fruitée et balsamique, rappelant la canelle avec une note d'ambre »[7].
Synthèse
La façon la plus simple de produire le cinnamate d'éthyle est évidemment l'estérification de l'acide cinnamique par l'éthanol.
Il est également possible de le produire par réaction entre l'acide cinnamique, le chlorure de thionyle (créant alors un intermédiaire chlorure de cinnamoyle) et d'éthanol[8].
Enfin, il est également possible de le produire par condensation de Claisen entre le benzaldéhyde et l'acétate d'éthyle.
Dérivés
Le dérivé p-methoxylé du cinnamate d'éthyle a été rapporté comme étant un inhibiteur de la monoamine oxydase[9].
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- Entrée de « Ethyl cinnamate » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 6 juin 2011 (JavaScript nécessaire)
- Fiche Sigma Aldrich, consultée le 6 juin 2011
- Voprosy Pitaniya. Problems of Nutrition. Vol. 33(5), Pg. 48, 1974
- K. C. et al. Wong, « Compositon of the essential oil of rhizomes of kaempferia galanga L. », dans Flavour and Fragrance Journal, vol. 7, no 5, 2006, p. 263–266 [lien DOI (page consultée le 2 juillet 2009)]
- R. et al. Othman, « Bioassay-guided isolation of a vasorelaxant active compound from Kaempferia galanga L. », dans Phytomedicine, vol. 13, no 1 - 2, 2006, p. 61–66 [lien PMID, lien DOI (pages consultées le 2 July 2009)]
- Budavari, Susan, « Merck Index 13th Ed. », dans Merck & co., Inc, 2001
- Autorengemeinschaft: Organikum, 15e édition, VEB Deutscher Verlag der Wissenschaften, Berlin 1976, S. 527.
- Noro T, Miyase T, Kuroyanagi M, Ueno A, Fukushima S., « Monoamine oxidase inhibitor from the rhizomes of Kaempferia galanga L. », dans Chem Pharm Bull (Tokyo)., vol. 31, no 8, 1983, p. 2708–11 [lien PMID]
- (en)/(de) Cet article est partiellement ou en totalité issu des articles intitulés en anglais « Ethyl cinnamate » (voir la liste des auteurs) et en allemand « Zimtsäureethyleste » (voir la liste des auteurs)
- Portail de la chimie
- Portail de la biochimie
- Portail de l’alimentation et de la gastronomie
- Portail des odeurs, des senteurs et du parfum
Catégories :- Phénylpropanoïde
- Ester d'éthyle
- Additif alimentaire
- Arôme
Wikimedia Foundation. 2010.
