- Oxydation de swern
-
Oxydation de Swern
L’oxydation de Swern est l'oxydation douce des alcools primaires et secondaires en aldéhyde et en cétone dans un milieu contenant du chlorure d'oxalyle, du diméthylsulfoxyde et de la triéthylamine.
L'avantage principal de cette méthode réside dans la douceur des conditions qui compense l'utilisation de réactifs toxiques (chlorure d'oxalyle, diméthylsulfoxyde, dégagement de monoxyde de carbone). Il est de plus impossible d'observer l'oxydation supplémentaire en acide carboxylique dans le cas de l'oxydation d'un alcool primaire. Cette méthode est très souvent utilisée dans la synthèse totale de produits naturels.
Les sous produits sont le sulfure de diméthyle (Me2S), le monoxyde de carbone (CO), le dioxyde de carbone (CO2) et - quand la triéthylamine est utilisée comme base - le chlorure de triéthylammonium (Et3NHCl). Deux d'entre eux, Me2S et CO sont très toxiques et volatiles: la réaction doit donc être réalisée sous hotte. Me2S est un liquide volatile (Teb = 37 °C) à l'odeur déplaisante: un moyen de limiter cette odeur est de le traiter à l'ozone pour le transformer en diméthylsulfoxyde, inodore.
Sommaire
Mécanisme
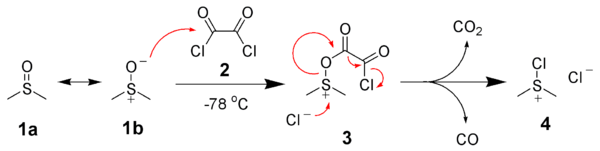
La première étape de l'oxydation de Swern est la réaction, à basse température, du diméthylsulfoxyde (DMSO) 1a et 1b avec le chlorure d'oxalyle, 2. Le premier intermédiaire, 3, se décompose rapidement, libérant des oxydes de carbone (CO et CO2) et produisant du chlorure de diméthylchlorosulfonium, 4.
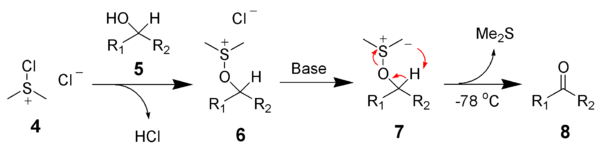
Après addition de l'alcool 5, le chlorure de diméthylchlorosulfonium 4 réagit avec l'alcool pour donner l'intermédiaire ionique alkoxysulfonium, 6. L'ajout d'au moins deux équivalents de base - typiquement la triéthylamine - va déprotoner l'ion alkoxysulfonium pour donner l'ylure de soufre, 7. Dans un état de transition comportant un cycle à 5 pièces, l'ylure de soufre se décompose pour donner le sulfure de diméthyle (Me2S) et l'aldéhyde ou la cétone recherchée, 8.
Variantes
Lorsqu'on utilise le chlorure d'oxalyle comme agent de déshydratation, la réaction doit être maintenue à une température inférieure à -60 °C pour éviter les réactions secondaires. En utilisant l'anhydride trifluoroacétique à la place du chlorure d'oxalyle, la température peut être augmentée à -30 °C sans réactions secondaires. On peut également activer le DMSO pour initier la formation de l'intermédiaire 6 avec des carbodiimides (oxydation de Pfitzner-Moffatt) ou un complexe trioxyde de piridine-soufre (oxydation de Parikh-Doering).
Dans certains cas, l'utilisation de triéthylamine en tant que base peut conduire à l'épimérisation du carbone α du carbonyle nouvellement formé. L'utilisation du diisopropyléthylamine (i-Pr2NEt, base de Hünig), plus encombrant, peut tempérer cet effet non désiré.
Remarque
Le sulfure de diméthyle, sous produit de cette réaction, a une odeur très désagréable. Les glandes olfactives humaines sont d'ailleurs capables de détecter ce composé dans des concentrations de l'ordre de quelques parts par milliard. Une solution simple à ce problème incommodant est de rincer la verrerie à l'eau de Javel, capable d'oxyder le sulfure de diméthyle et ainsi d'éliminer l'odeur.
Voir aussi
- Oxydation et réduction en chimie organique
- Oxydation d'un alcool
- Chlorochromate de pyridinium
- Réactif de Collins
- Oxydation de Jones
- Oxydation de Sarett
- Portail de la chimie
Catégorie : Réaction d'oxydo-réduction organique
Wikimedia Foundation. 2010.