- E 400
-
Alginate
Alginate 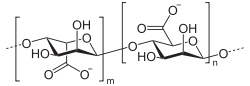
Alginate
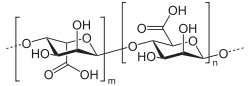
Acide alginiqueGénéral Nom IUPAC (2R,3S,4R,5R,6S)-6-[(2R,3R,4R,5R,6S)-2-carboxy-4, 5-dihydroxy-6-methoxyoxan-3-yl]oxy-4, 5-dihydroxy-3-methoxyoxane-2-carboxylic acid Synonymes Acide alginique No CAS No EINECS Code ATC A02 PubChem No E E400 SMILES InChI Propriétés chimiques Formule brute (C6H8O6)n Masse molaire 176,1241 g∙mol-1
C 40,92 %, H 4,58 %, O 54,5 %,Écotoxicologie DL50 >5000mg/kg rat oral
1600mg/kg rat i.p. [1]Unités du SI & CNTP, sauf indication contraire. Les alginates sont des polysaccharides obtenus à partir d'une famille d'algues brunes : les laminaires.
Ils peuvent former des gels durs et thermostables utilisés comme additifs alimentaires (E400 à E405) permettant la reconstruction des aliments (jambon, cordons bleus, le poisson pané…). Les alginates donnent une texture onctueuse à nombre d'aliments tels que les crèmes glacées. Les alginates alcalins forment dans l'eau des solutions colloïdales visqueuses tandis que l'alginate de calcium est insoluble comme l'acide alginique lui-même. Les alginates sont utilisés comme épaississants, gélifiants, émulsifiants et stabilisants de produits industriels les plus variés depuis les gelées alimentaires, les produits de beauté, jusqu'aux peintures et aux encres d'imprimerie. Les laits gélifiés le sont par des alginates et carraghénanes, qui produisent des desserts lactés pasteurisés.
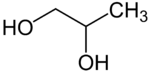
Des billes d'alginates peuvent également être utilisées en médecine pour encapsuler des médicaments ou des substances biologiques fragiles (enzymes, microorganismes, cellules animales ou humaines). L'alginate de propane-1,2-diol (E405), ester de l'acide aliginique, est utilisé, par exemple, pour stabiliser des mousses (vinification, additif de bière ...), et est également utilisé dans un procédé de préparation de microcapsules.
L'alginate est également utilisé pour réaliser des moulages sur le corps humain grâce à ses qualités hypoallergéniques. C'est souvent le produit utilisé par les dentistes pour les prises d'empreintes dentaires. Sa couleur varie du blanc crème à l'ivoire foncé. Sa granulométrie très fine permet des empreintes très fidèles.
Il est aussi utilisé par les spécialistes des effets spéciaux au cinéma pour reproduire des parties du corps humain.
L'acide alginique a été découvert par E. C. Stanford, un pharmacien britannique dans les années 1880.Il est tiré des algues et permet la production de fibres d'alginates de sodium et de calcium. L'alginate de sodium est très soluble dans l'eau, l'alginate de calcium est seulement soluble en milieu basique, notamment en solutions de savon qui sont presque toujours assez alcalines : d'où l'utilisation de ces fibres comme soutiens passagers, qui seront à éliminer après fabrication, par lavage ou par foulonnage. Pour transformer les articles en alginates insolubles, on les utilise sous forme de sels de béryllium ou de chrome.
Sommaire
Composition chimique
L'alginate est un polymère formé de deux monomères liés ensemble : le mannuronate ou acide mannuronique dont certains sont acétylés et le guluronate ou acide guluronique. La proportion et la distribution de ces deux monomères sont déterminante pour une large expansion des propriétés physiques et chimiques de l'alginate. Sa composition chimique varie selon les diverses espèces d'algues, les différentes parties de la même plante et est sujette aux changements saisonniers. Néanmoins par sélection de matières premières aux différentes propriétés, il est possible de fabriquer une variété d'alginate aux caractéristiques constantes.
Procédé de fabrication
L'algue est coupée et nettoyée après la récolte. Puis elle est mise à macérer dans un acide minéral dilué pour être déminéralisée. L'alginate contenu dans l'algue est ainsi transformé en acide alginique et, en même temps, certains constituants indésirables sont éliminés[2]. Les algues déminéralisées sont broyées en présence d'un alcali ou d'un sel alcalin afin de neutraliser l'acide alginique et de solubiliser celui-ci sous forme de sel correspondant. L'alginate est extrait et traité. Il est précipité, pressé, lavé et essoré, puis neutralisé, séché et moulu à la granulométrie désirée. On obtient alors différents sels aux propriétés bien précises : les alginates de métaux alcalins (sodium, potassium, magnésium...) sont solubles dans l'eau tandis que l'acide alginique et son dérivé calcique (calcium, aluminium, fer...) y sont pratiquement insolubles. Les sels solubles se dilsolvent à basse température et forment des solutions épaisses et visqueuses, des gels résistants à la chaleur.
Références
- ↑ ChemIDPlus. Consulté le 3 février 2009
- ↑ Les algues : une « agroressource » d'avenir Des expériences autour des algues décrites sur CultureSciences Chimie, un site ENS-DGESCO
Bibliographie
- Techniques et pratique du staff aux éditions-eyrolles.com
- Portail de la chimie
Catégories : Texturant alimentaire | Dent | Effets spéciaux | Polyoside | Phycologie
Wikimedia Foundation. 2010.