1,4-cyclohexanedione
- 1,4-cyclohexanedione
-
| 1,4-cyclohexanedione |
|
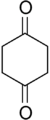
structure de la 1,4-cyclohexanedione |
| Général |
| Nom IUPAC |
cyclohexane-1,4-dione |
| Synonymes |
tétrahydroquinone |
| No CAS |
637-88-7 |
| No EINECS |
211-306-0 |
| PubChem |
12511 |
| ChEBI |
28286 |
| SMILES |
|
| InChI |
InChI : Vue 3D
InChI=1S/C6H8O2/c7-5-1-2-6(8)4-3-5/h1-4H2
|
| Propriétés chimiques |
| Formule brute |
C6H8O2 [Isomères]unité C6H8O2 |
| Masse molaire[1] |
112,1265 ± 0,006 g·mol-1
C 64,27 %, H 7,19 %, O 28,54 %,
|
| Propriétés physiques |
| T° fusion |
76,85 °C [2] |
| T° ébullition |
112 °C |
| Thermochimie |
| ΔfH0gaz |
-332,6 kJ·mol-1 [2] |
| ΔfH0solide |
-407,6 kJ·mol-1 [2] |
| Cp |
161,4 J·mol-1·K-1 (26,85 °C,solide)[2] |
|
Unités du SI & CNTP, sauf indication contraire.
|
La 1,4-cyclohexanedione est un composé chimique de formule C6H8O2. C'est l'un des trois isomères de cyclohexanediones ; cette dicétone est utilisée comme précurseur dans la synthèse de molécules plus complexes.
Production et synthèse
La 1,4-cyclohexanedione est préparée en deux étapes à partir de diesters d'acide succinique HOOC–CH2–CH2–COOH. Deux molécules de succinate de diéthyle H3C–CH2–OOC–CH2–CH2–COO–CH2–CH3 se condensent en milieu acide pour donner une molécule de 2,5-dicarbéthoxy-1,4-cyclohexanedione, dont les deux groupes –COO–CH2–CH3 sont subséquemment éliminés par hydrolyse pour donner la 1,4-cyclohexanedione[3].
Notes et références
- ↑ Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- ↑ a, b, c et d (en) « 1,4-Cyclohexanedione » sur NIST/WebBook, consulté le 17 juin 2009
- ↑ Arnold T. Nielsen, Wayne R. Carpenter, William G. Dauben, E. John Deviny, « 1,4-Cyclohexanedione », dans Organic Syntheses, vol. 5, 1973, p. 288 [texte intégral (page consultée le 13/06/2009)]
Wikimedia Foundation.
2010.
Contenu soumis à la licence CC-BY-SA. Source : Article 1,4-cyclohexanedione de Wikipédia en français (auteurs)
Regardez d'autres dictionnaires:
1,4-Cyclohexanedione — 1,4 Cyclohexanedione[1] IUPAC name … Wikipedia
637-88-7 — 1,4 cyclohexanedione 1,4 cyclohexanedione structure de la 1,4 cyclohexanedione Général Nom IUPAC cyclohex … Wikipédia en Français
Wieland-Miescher ketone — Chembox new Reference= [ [http://www.sigmaaldrich.com/catalog/search/ProductDetail/ALDRICH/M65157?cm mmc=PubChem public%20database products products (±) 8a Methyl 3,4,8,8a tetrahydro 1,6(2H,7H) naphthalenedione] at Sigma Aldrich]… … Wikipedia
Nitisinone — Systematic (IUPAC) name 2 [2 nitro 4 (trifluoromethyl)benzoyl] cyclohexane 1,3 dione Clinical data AHFS/Drugs.com … Wikipedia
Dimedone — IUPAC name … Wikipedia
Annulation de Robinson — ██████████90 … Wikipédia en Français
Hydrogenation — |date=1996|location=Washington, D.C.|pages=429|id=ISBN 0 8412 3344 6] Because of the importance of hydrogen, many related reactions have been developed for its use. Most hydrogenations use gaseous hydrogen (H2), but some involve the alternative… … Wikipedia
Michael reaction — The Michael reaction or Michael addition is the nucleophilic addition of a carbanion or another nucleophile[1][2][3] to an alpha, beta unsaturated carbonyl compound. It belongs to the larger class of conjugate additions. This is one of the most… … Wikipedia
Robinson annulation — The Robinson annulation is an organic reaction used to create a six member ring α,β unsaturated cyclic ketone, using a ketone (or aldehyde) and methyl vinyl ketone. [Rapson, W. S.; Robinson, R.; J. Chem. Soc. 1935, 1285.] [Bergmann, E. D.;… … Wikipedia
Selenium dioxide — Selenium dioxide … Wikipedia

