- Annulation de Robinson
-
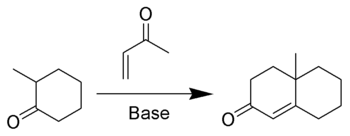
En chimie organique, l'annulation de Robinson est une réaction qui créé une cétone α,β-insaturée cyclique à 6 membres à partir d'une cétone (ou aldéhyde) et de la méthylvinylcétone[1],[2],[3]. La réaction tient son nom du chimiste britannique Robert Robinson qui l'a découverte à l'université d'Oxford.
Sommaire
Mécanisme
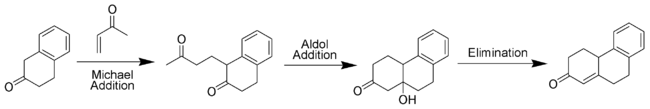
La méthylvinylcétone (ou ses dérivés) est un réactif essentiel de la réaction puisqu'elle est à la fois un accepteur de Michael et qu'elle peut prendre part à une condensation aldolique. La première étape de l'annulation est une addition de Michael suivie par une addition aldolique comme étape de cyclisation. La réaction continue par une étape de déshydratation comme dans une condensation aldolique classique pour former le cycle cyclohexènone.
Variantes
Annulation de Robinson asymétrique
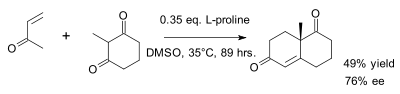
L'original de Wieland-Miescher cétone est racémique et préparés dans un Robinson annulation de 2-méthyl-1 ,3-cyclohexanedione et la méthyl vinyl cétone[4]. L'annulation de Robinson peut être rendue stéréoselective par l'ajout de L- ou D-proline[5].
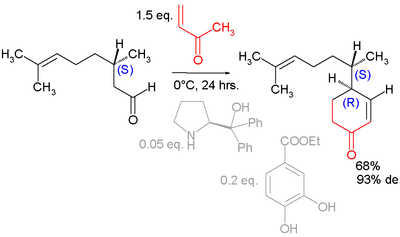
Des dérivés de la proline peuvent aussi être utilisés comme pour cette annulation asymétrique du géranial[6] :
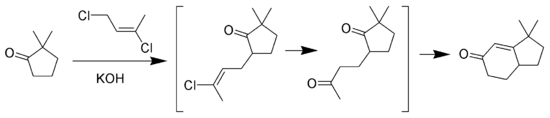
Réaction de Wichterle
La réaction de Wichterle est une variante de l'annulation de Robinson où la méthylvinylcétone est remplacée par le 1,3-dichloro-cis-2-butène[7],[8],[9].
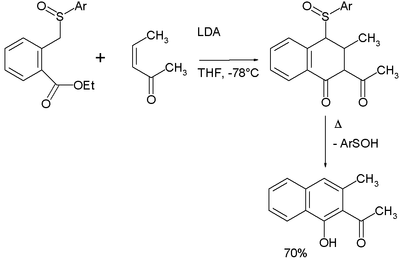
Annulation de Hauser
La séquence réactionnelle de l'annulation de Hauser est addition de Michael - condensation de Dieckman - élimination[10].
Applications
La cétone de Wieland-Miescher est le produit de l'annulation de Robinson de la 2-méthyl-1,3-cyclohexanedione et de la méthylvinylcétone alors que la cétone de Hajos-Parrish est le produit de la réaction de la 2-méthyl-1,3-cyclopentanedione et de la méthylvinylcétone suivi par D-proline a catalysé la formation d'anneau[11].
Notes et références
- William Sage Rapson, « 307. Experiments on the synthesis of substances related to the sterols. Part II. A new general method for the synthesis of substituted cyclohexenones », dans Journal of the Chemical Society (Resumed), 1935, p. 1285 [lien DOI]
- Bergmann, E. D.; Ginsberg, D.; Pappo, R. Org. React. 1959, 10, 179. (Review)
- Robert E. Gawley, « The Robinson Annelation and Related Reactions », dans Synthesis, vol. 1976, 1976, p. 777 [lien DOI]
- Wieland, P.; Miescher, K.: In Über die Herstellung mehrkerniger Ketone., Helv. Chim. Acta 1950, 33, 2215. DOI:10.1002/hlca.19500330730
- Hajos,Zoltan G., Parrish,David R. le brevet allemand DE 2102623 (29 Juillet 1971) et USP 3.975.440 (Aug.17, 1976) Exemple 21.
- Total Synthesis and Revised Structure of Biyouyanagin A K. C. Nicolaou, David Sarlah, and David M. Shaw Angew. Chem. Int. Ed. 2007, 46, 4708 –4711 DOI:10.1002/anie.200701552
- Wichterle, O. et al. Coll. Czech. Chem. Commun. 1948, 13, 300.
- Kobayashi, M.; Matsumoto, T. Chem. Lett. 1973, 957.
- Organic Syntheses, Coll. Vol. 5, p.869 (1973); Vol. 45, p.80 (1965). (Article)
- Recent Advances in the Hauser Annulation Mal, D.; Pahari, P. Chem. Rev.; (Review); 2007; 107(5); 1892-1918. DOI:10.1021/cr068398q
- Asymmetric synthesis of bicyclic intermediates of natural product chemistry Zoltan G. Hajos, David R. Parrish J. Org. Chem.; 1974; 39(12); 1615-1621
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Robinson annulation » (voir la liste des auteurs)
- (de) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en allemand intitulé « Robinson-Anellierung » (voir la liste des auteurs)
Wikimedia Foundation. 2010.