- DCCNa
-
Dichloroisocyanurate de sodium
Dichloroisocyanurate de sodium 
Structure chimique du dichloroisocyanurate de sodium Général Nom IUPAC sodium 3,5-dichloro-2,4,6-
trioxo-1,3,5-triazinan-1-ideNo CAS No EINECS PubChem SMILES InChI Apparence poudre cristalline blanche, d'odeur âcre.[1] Propriétés chimiques Formule brute C3Cl2N3NaO3 [Isomères] Masse molaire 219,946 g∙mol-1
C 16,38 %, Cl 32,24 %, N 19,1 %, Na 10,45 %, O 21,82 %,Propriétés physiques T° fusion Se décompose au-dessous du point de fusion à 230 °C[1] Solubilité dans l'eau : 25 g/100 ml[1] Masse volumique >1 Pression de vapeur saturante <0.00005 mm Hg Précautions Directive 67/548/EEC 
Xn
O
NPhrases R : 8, 22, 31, 36/37, 50/53, Phrases S : 8, 26, 41, 60, 61, Transport 50 2465 [2]NFPA 704 SIMDUT[4] 

SGH[5] 


DangerInhalation Toux. Mal de gorge.[3] Peau Rougeur. Brûlures cutanées.
Douleur.[3]Yeux Rougeur. Douleur. Perte de la vue.
Brûlures profondes graves.[3]Ingestion Sensation de brûlure. Mal de gorge.[3] Écotoxicologie CL50 0.27 à 1.17 mg/l (rats) Unités du SI & CNTP, sauf indication contraire. Le dichloroisocyanurate de sodium (ou DCCNa) est une source stable de chlore libre. Il est utilisé comme désinfectant, biocide, désodorisant industriel.
Il constitue le chlore choc utilisé pour la désinfection de l'eau des piscines. (Le chlore lent correspond à l'acide trichloroisocyanurique).
C'est un sel de sodium de l'acide dichloroisocyanurique, soluble dans l'eau. De couleur blanche, il est proposé en granules, poudre ou pastilles de 20 g. Ce composé hétérocyclique dérive de la triazine.
Il réagit avec l'eau, l'urée, l'ammoniac, les agents réducteurs et les bases fortes.
Dans l'eau, il se décompose en acide hypochloreux (le désinfectant et oxydant que produit l'eau de javel) et en cyanurate de sodium, qui joue un rôle de stabilisant en protégeant l'acide hypochloreux HClO et l'ion hypochlorite ClO- d'une décomposition par les ultra-violets.
- C3Cl2N3O3Na + 2·H2O → C3H3N3O3 + HClO + Na+ + ClO-
Il n'a pas d'effet significatif sur le pH de l'eau. Il faut privilégier un pH de l'ordre de 7.4 (7.2-7.5) favorable à la formation de l'acide hypochloreux. Par exemple, avec un pH de 8.2, il faudrait 2 mg/l pour avoir le même effet bactéricide que 0.7 mg/l à pH = 7.4.[6]
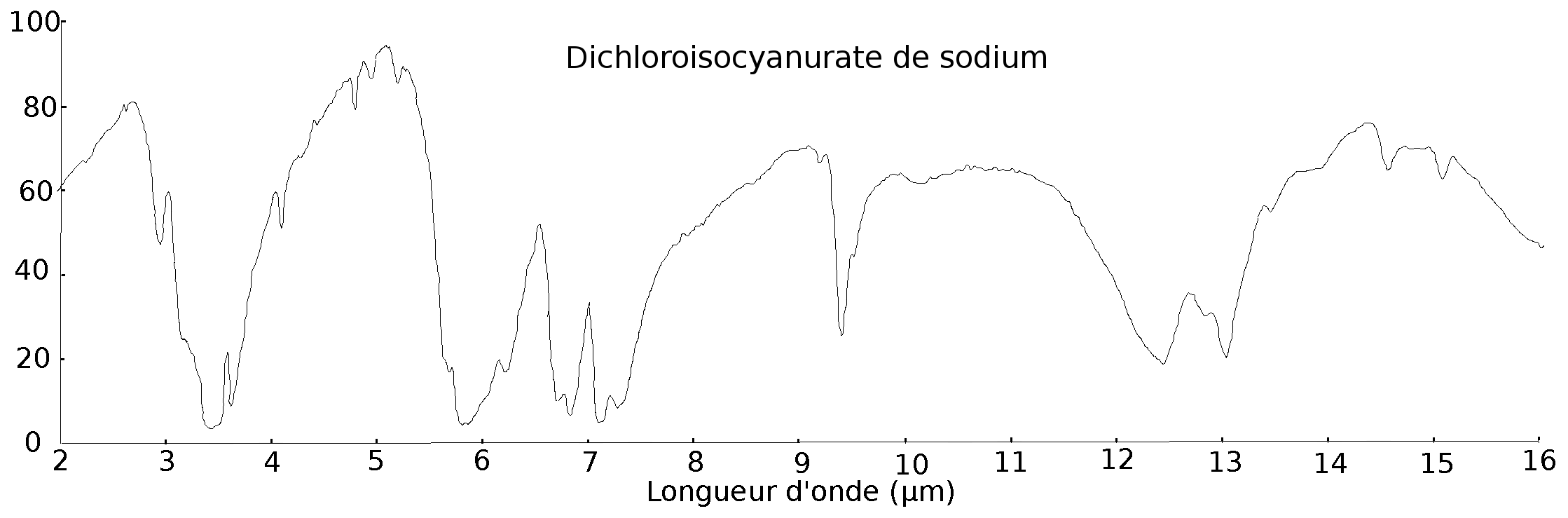 Spectre infrarouge
Spectre infrarouge
Sécurité
Maintenir hors de portée des enfants. Stocker impérativement dans des locaux bien ventilés, à l'abri de l'humidité et de toute source de chaleur ou d'ignition. Séparer des aliments et des produits alimentaires et des matières incompatibles[3]. Conserver au sec. Bien fermer.
Pour les conditions de stockage et d'utilisation, se reporter à la Circulaire DGS/SD 7 A/DRT/CT 4 n° 2003-47 du 30 janvier 2003 relative aux risques d'incendie ou d'explosion lors du stockage et/ou de l'utilisation de produits de traitement des eaux de piscine.
- en cas d'ingestion : Rincer la bouche. NE PAS faire vomir. Mettre au repos. Consulter un médecin.[3]
- en cas de contact avec les yeux : Rincer d'abord abondamment à l'eau pendant plusieurs minutes (retirer si possible les lentilles de contact), puis consulter un médecin.[3]
- en cas de contact avec la peau : Retirer les vêtements contaminés. Rincer la peau abondamment à l'eau ou prendre une douche. Consulter un médecin.[3]
Notes et références
- ↑ a , b et c DICHLOROISOCYANURATE DE SODIUM, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ Entrée du numéro CAS « 2893-78-9 » dans la base de données de produits chimiques GESTIS de la BGIA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 27 novembre 2008 (JavaScript nécessaire)
- ↑ a , b , c , d , e , f , g et h Fiches internationales de sécurité chimique Dichloroisocyanurate de sodium
- ↑ « Dichloroisocyanurate de sodium » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- ↑ Arpège : Le traitement des eaux de piscine
- Portail de la chimie
Catégories : Composé du sodium | Produit chimique nocif | Produit chimique comburant | Produit chimique dangereux pour l'environnement | Triazine | Chloramine | Cétone
Wikimedia Foundation. 2010.


