- Chélatant
-
Chélation
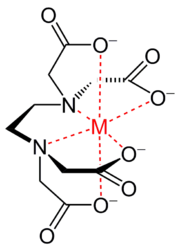 Complexe chélate de l'EDTA avec un cation métallique
Complexe chélate de l'EDTA avec un cation métallique
La chélation (prononcer kélassion, du grec khêlê : « pince ») est un processus physico-chimique au cours duquel est formé un complexe, le chélate, entre un ligand, dit chélateur (ou chélatant), et un cation (ou atome) métallique, alors complexé, dit chélaté.
Le « chélate » se distingue du simple « complexe » par le fait que le cation métallique est fixé au chélateur par au moins deux liaisons de coordination définissant un cycle avec le métal, à la manière d'une pince, d'où le nom. Le nombre de liaisons métal-ligand qu'il est possible de former définit la « denticité » : on parle de coordinats bidentes, tridentes, tétradentes, etc, ainsi que de ligands monodentates, bidentates, polydentates. L’atome central est lié aux atomes voisins par au moins deux liaisons en formant une structure annulaire, un cycle chélate. Les cycles chélates les plus stables sont les cycles chélates à 5 et à 6 chaînons. Grâce à cet effet, les chélates sont des complexes plus stables que les complexes de ligands monodentes comportant les mêmes fonctions chimiques.
Sommaire
Typologie des chélateurs
Il existe des chélatants faibles, qui forment des complexes labiles et instables, et des chélatants forts, tels l'EDTA, qui peuvent former des complexes extrêmement stables et inertes, caractérisés par des constantes de dissociation inférieures à 10-27, c'est-à-dire que la forme complexée est un milliard de milliard de milliard de fois plus stable que la forme dissociée.
Fonctions biologiques
La chélation est un phénomène naturel fondamental
- en chimie bioinorganique : par exemple les ions de cobalt dans la vitamine B12, de magnésium dans la chlorophylle, de cuivre dans l'hémocyanine ou de fer dans l'hémoglobine sont chélatés.
- en biologie : la plupart des organismes vivant produisent des protéines spéciales (métallothionéines), riches en soufre qui contribuent à détoxiquer l'organisme.
- Chez l'homme, les individus le font plus ou moins efficacement selon leur patrimoine génétique. Ceux dont l'organisme ne se détoxique pas assez vite ont plus de risque de développer des maladies neurodégénératives (Maladie d'Alzheimer (MA) notamment), en particulier en cas d'exposition au mercure inorganique perdu par les plombages dentaires. Chez les personnes génétiquement moins apte à sa détoxication le mercure augmente quantitativement et ses effets toxiques sont aggravés (hydrargyrisme).
remarque : la suceptibilité génétique au mercure est (liée au polymorphisme du gène de l’apolipoprotéine E ou APOE ; Elle est corrélée à un risque beaucoup plus élevé de développer une MA, et de la développer plus jeune [1],[2]). Un trouble cognitif léger a aussi plus de valeur prédictive chez ces derniers[3]. Ce gène APOE existe sous 3 formes (allèles APOE2, APOE3 et APO4). L'APOE 2 est plutôt protecteur, alors que l'APOE4 expose au risque maximal (y compris pour l'âge) [4],[5],[6]. Par exemple, un caucasien homozygote pour APOE2 a 25 fois moins de risques de MA que son homologue homozygote pour APOE4 (OR =0,6 vs 14,9).
Applications
Les applications des chélateurs sont nombreuses, par exemple :
- en médecine:Lors d'une intoxication avec des poisons métalliques ou contamination interne par des produits radiologiques (plutonium, américium, berkelium, curium, yttrium, californium...), cette propriété est mise à profit avec des antidotes - par exemple du Zn-DTPA ou Ca-DTPA - qui forment un chélate éliminé lors de la miction. Cette capacité de soustraire les cations métalliques du milieu est appelée séquestration : on donne donc aussi aux chélateurs le nom d'agents séquestrants.
- en chimie analytique,
- dans l'industrie nucléaire,
- dans la teinturerie,
- dans la métallurgie,
- en agronomie. Ces agents peuvent soit passiver une surface métallique (comme le cuivre) par complexation (liaison pendante en surface) soit éloigner les ions métalliques de la surface.
Il existe aussi des chélateurs naturels telles que des molécules contenues dans la bardane, l'ail, le lierre terrestre, les algues et la coriandre[réf. nécessaire].
Notes et références de l'article
- ↑ Blacker D, Haines JL, Rodes L, Terwedow H, Go RC, Harrell LE, Perry RT, Bassett SS, Chase G, Meyers D, Albert MS, Tanzi R. ApoE-4 and age at onset of Alzheimer's disease: the NIMH genetics initiative. 1: Neurology. Janvier 1997 Jan ; 48(1):139-47
- ↑ Olarte L, Schupf N, Lee JH, Tang MX, Santana V, Williamson J, Maramreddy P, Tycko B,Mayeux R.Apolipoprotein E epsilon4 and age at onset of sporadic and familial Alzheimer disease in Caribbean Hispanics. ; Arch Neurol. Novembre 2006 ; 63(11):1586-90
- ↑ Aggarwal NT, Wilson RS, Beck TL, Bienias JL, Berry-Kravis E, Bennett DA. ; The apolipoprotein E epsilon4 allele and incident Alzheimer's disease in persons with mild cognitive impairment. Neurocase. Février 2005 ; 11(1):3-7
- ↑ Huang Y. ; Apolipoprotein E and Alzheimer disease. ; Neurology. 2006 Jan 24;66(2 Suppl 1):S79-85
- ↑ Slooter AJ, Cruts M, Kalmijn S, Hofman A, Breteler MM, Van Broeckhoven C, van Duijn CM Arch Neurol ; Risk estimates of dementia by apolipoprotein E genotypes from a population-based incidence study : the Rotterdam Study. Juillet 1998 ; 55(7):964-8
- ↑ Effects of age, sex, and ethnicity on the association between apolipoprotein E genotype and Alzheimer disease. A meta-analysis. APOE and Alzheimer Disease Meta Analysis Consortium.Farrer LA, Cupples LA, Haines JL, Hyman B, Kukull WA, Mayeux R, Myers RH, Pericak-Vance MA, Risch N, van Duijn CM JAMA. Octobre 1997 ; 2-29;278(16):1349-56.
Voir aussi
Articles connexes
Liens et documents externes
- (en) Descripton et utilisation de trisodium calcium diethylenetriaminepentaacetate dans l'élimination des produits transuraniques par chélation [1]. Radiation Emergency Assistance Center/Training Site
- (fr) Traitement d'ouvriers contaminés par des produits radiologiques avec des infusions de Ca-DPTA. Radioprotection 2004, Vol. 39, n° 3, pages 383 à 387 [2]
- Portail de la chimie
Catégorie : Chélation
Wikimedia Foundation. 2010.
