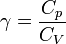- Chaleur massique
-
Capacité thermique massique
La chaleur massique ou chaleur spécifique[1] (symbole c ou s), qu'il convient d'appeler capacité thermique massique, est déterminée par la quantité d'énergie à apporter par échange thermique pour élever d'un degré la température de l'unité de masse d'une substance. C'est donc une grandeur extensive égale à la capacité thermique rapportée à la masse du corps étudié.
L'unité du système international est alors le joule par kilogramme-kelvin (J·kg-1·K-1). La détermination des valeurs des capacités thermiques des substances relève de la calorimétrie.
Suivant le type de transformation thermodynamique, on considère soit l'énergie interne massique, soit l'enthalpie massique. Si on note U l'énergie interne, H l'enthalpie et m la masse d'un corps on a donc les capacités thermiques massiques :
- à volume constant :
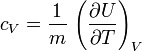 ;
; - à pression constante :
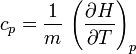 .
.
La différence entre la chaleur spécifique à pression constante cp et la chaleur spécifique à volume constant cV est liée au travail qui doit être fourni pour dilater le corps en présence d'une pression externe. Si elle est souvent négligeable pour les phases condensées réputées peu compressibles et peu dilatables (liquides ou solides) la différence entre cV et cp est importante pour les gaz.
Sommaire
Cas des gaz parfaits
D'après la théorie cinétique des gaz, l'énergie interne d'une mole de gaz parfait monoatomique est égale à (3/2)RT, et plus élevée pour les gaz dont les molécules sont polyatomiques ; par exemple, (5/2)RT pour un gaz diatomique. Le calcul théorique n'est plus possible pour les molécules complexes.
La capacité massique à volume constant est ainsi de :
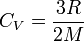 pour un gaz parfait monoatomique ;
pour un gaz parfait monoatomique ;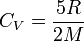 pour un gaz parfait diatomique.
pour un gaz parfait diatomique.
La capacité massique à pression constante d'un gaz parfait peut être déterminée à partir de la capacité massique à volume constant, puisque l'équation des gaz parfaits exprime que :
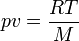 , et donc :
, et donc : 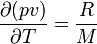
p étant la pression, v le volume massique[2], R la constante molaire des gaz[3], et M la masse molaire du gaz considéré.
La différence théorique entre ces deux valeurs est ainsi :
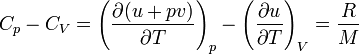 , u ne dépendant que de la température.
, u ne dépendant que de la température.Le rapport des deux capacités d'un gaz est important en thermodynamique ; il est noté gamma :
Sa valeur dépend de la nature du gaz considéré ; pour un gaz parfait, la valeur théorique de γ est :
- γ = 5/3= 1,67 pour un gaz monoatomique (1/(γ-1)=3/2=1,5) ;
- γ = 7/5= 1,4 pour un gaz diatomique (1/(γ-1)=5/2=2,5).
Capacité thermique massique de gaz à volume constant[4], sous atmosphère normale Gaz Masse molaire
(kg/mol)température
(°C)capacité massique
J/(kg.K)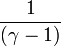
Air 29×10-3 0-100 710 2,48 Argon 39,948×10-3 15 320 1,54 Azote 28,013×10-3 0-200 730 2,46 Dioxyde de carbone 44,01×10-3 20 650 3,44 Hélium 4,003×10-3 18 3160 1,52 Hydrogène 2,016×10-3 16 10140 2,46 Oxygène 31,999×10-3 13-207 650 2,50 Vapeur d'eau 18,015×10-3 100 1410 3,06 Cas des solides
substance (phase solide)
Capacité thermique massique J·kg-1·K-1
asphalte 920 brique 840 béton 880 granite 790 gypse 1090 marbre 880 sable 835 bois 420 Dans le cas des solides, à suffisamment haute température, la loi de Dulong et Petit est applicable et permet notamment retrouver que, à basse température,
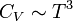 du fait de la contribution des phonons. Si le solide est un métal, il faut ajouter la contribution des électrons qui est proportionnelle à la température.
du fait de la contribution des phonons. Si le solide est un métal, il faut ajouter la contribution des électrons qui est proportionnelle à la température.Les coefficients de dilatation des corps solides et liquides sont généralement suffisamment faibles pour qu'on néglige la différence entre Cp et CV pour la plupart des applications.
Substance Θ (K) Al 398 C (diamant) 1860 Cu 315 Fe 420 K 99 Pb 88 Suivant la théorie de Debye, la capacité thermique molaire d'un corps simple solide peut être déterminée au moyen de la formule :
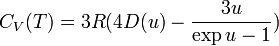
avec
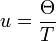 ,
,Θ est la température de Debye, qui est une caractéristique de chaque substance,
R est la constante molaire des gaz[3],
et
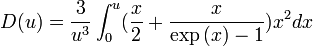 .
.Cette formule se simplifie à basse température, ainsi qu'à haute température ; dans ce dernier cas, nous retrouvons la loi de Dulong et Petit :
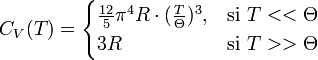
La théorie n'est plus valable pour les corps composés.
Pour des corps purs (solides, liquides ou gazeux) et à pression constante, 2 formules empiriques à 3 paramètres ont pu être dégagées, pour un intervalle de température donné :
Cp = a + bT + cT2 ou bien Cp = a' + b'T + c'T − 2.
Les valeurs des coefficients sont indiqués dans des tables et sont caractéristiques d'un corps donné.
Mesure de la capacité thermique massique d'un solide
La capacité thermique massique d'un solide peut être mesurée en utilisant un appareil de type ATD (analyse thermodifférentielle, ou DSC pour differential scanning calorimetry). Elle peut se définir de la façon suivante : quand un système passe de la température T à une température T+dT, la variation d’énergie interne du système dU est liée à la quantité de chaleur échangée δQ selon :
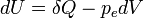
avec pe la pression extérieure à laquelle est soumis le système et dV la variation de volume. Si V=Cte:
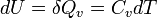
En revanche, si la transformation est isobare (pression constante), on obtient en utilisant la fonction enthalpie du système, la relation :
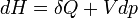
Si P= cte
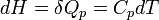
avec Cp la capacité à pression constante. La mesure consiste donc à mesurer la différence de température créée par un échange thermique donné, ou le flux d'énergie se traduit par une différence de température.
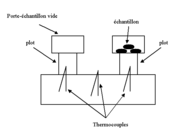
Le schéma suivant illustre la technique instrumentale utilisée dans le cas de la première méthode (mesure de la différence de température).
L’appareil est constitué de deux « plots » indépendants et d’un four. Des thermocouples permettent de mesurer la température de la face supérieure des plots en contact avec l’échantillon, ainsi que la température du four. Celle-ci correspond à la température de mesure. Toutes les mesures sont effectuées en utilisant un porte-échantillon d’aluminium vide sur l’un des plots. Une première mesure d’un autre porte-échantillon d’aluminium vide permet d’obtenir une ligne de base (dépendant de la mesure de température par les thermocouples). Puis une mesure d’un échantillon de référence de chaleur massique connue permet d’étalonner l’appareil. Enfin, l’échantillon sous forme de poudre est mesuré et sa chaleur massique est obtenue par comparaison avec celle de l’échantillon de référence. Pour améliorer la précisions de la mesure, il convient de prendre en compte le cas échéant la différence de masse entre les deux porte échantillons (la correction s'effectue en utilisant la chaleur massique de l'aluminium). La source d’erreur principale provient de la qualité du contact thermique entre le plot et le porte-échantillon.
Valeurs pour différentes substances
Capacité thermique massique à pression constante dans les conditions normales de température et de pression (sauf indication contraire) Substance Phase Capacité thermique
massique
J·kg-1·K-1Air (sec) gaz 1005 Air (saturé en vapeur d'eau) gaz ≈ 1030 Aluminium solide 897 Azote gaz 1042 Cuivre solide 385 Diamant solide 502 Eau gaz 1850 liquide 4186 solide (0 °C) 2060 Éthanol liquide 2460 Fer solide 444 Graphite solide 720 Hélium gaz 3160 Hexane liquide ≈ 2267.95 Huile liquide ≈ 2000 Hydrogène gaz 14300 Laiton solide 377 Lithium solide 3582 Mercure liquide 139 Octane liquide ≈ 1393.33 Or solide 129 Oxygène gaz 920 Zinc solide 380 Notes
- ↑ On rencontre parfois le terme spécifique, dans le même sens que massique. C'est un calque de l'anglais specific heat désignant le terme français chaleur massique
- ↑ Le volume massique est la grandeur inverse de la masse volumique.
- ↑ a et b R = 8,314 4 J/K/mol.
- ↑ À la différence du premier tableau où on donne la capacité massique à pression constante..
Voir aussi
Bibliographie
- J. Boutigny, Thermodynamique, Vuibert.
- Lev Landau et Evguéni Lifchitz, Physique théorique, tome 5 : Physique statistique, éd. MIR, Moscou [détail des éditions]
- Charles Kittel (trad. Nathalie Bardou, Évelyne Kolb), Physique de l’état solide [« Solid state physics »], 1998 [détail des éditions]
- Portail de la physique
Catégories : Grandeur physique | Thermodynamique - à volume constant :
Wikimedia Foundation. 2010.