- 96-48-0
-
Gamma-butyrolactone
Gamma-butyrolactone 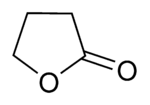
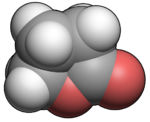
Structure du gamma-butyrolactone Général Nom IUPAC gamma-butyrolactone Synonymes Tétrahydro-2-furanone
Dihydro-2(3H)-furanoneNo CAS No EINECS FEMA Apparence liquide hygroscopique, incolore, huileux.[1] Propriétés chimiques Formule brute C4H6O2 [Isomères] Masse molaire 86,0892 g∙mol-1
C 55,81 %, H 7,02 %, O 37,17 %,Propriétés physiques T° fusion -44 °C[1] T° ébullition 204 °C[1] Solubilité dans l'eau : miscible Masse volumique (eau = 1) : 1.1[1] T° d’auto-inflammation 455 °C[1] Point d’éclair 98 °C c.f.[1] Limites d’explosivité dans l’air en volume % dans l'air : 0.3-16.0[1] Pression de vapeur saturante à 20 °C : 0.15 kPa[1] Précautions NFPA 704 Classification du CIRC Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[2] Écotoxicologie LogP -0.57[1] Caractère psychotrope Catégorie Dépresseur Mode de consommation Ingestion Autres dénominations GBL
gamma butyrolacétoneComposés apparentés Isomère(s) Diacétyle Unités du SI & CNTP, sauf indication contraire. Le gamma-butyrolactone (GBL) est un précurseur de l'acide gamma-hydroxybutyrique (GHB). Il est utilisé dans l'industrie comme solvant à peinture, époxy ou vernis à ongles où ses caractéristiques très acides font fondre le plastique, décapent et blanchissent les vernis.
Sommaire
Effet sur l'organisme
Dans le corps humain, le gamma-butyrolactone[3] se transforme in vivo en GHB ; c'est pour cela qu'il produit les mêmes effets que le GHB : euphorie, production d'hormone de croissance, relaxation, augmentation de la libido ; coma potentiellement mortel en cas d'overdose. Ce solvant peut être détourné en drogue[4].
Son caractère hautement acide impose une haute dilution préalable à toute consommation et c'est pourquoi le GHB (également appelé drogue du violeur) lui est préféré car il est nettement moins dangereux.
Relation chimique entre GBL et GHB
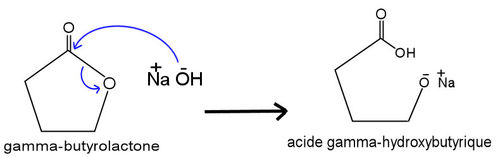
L'ouverture du cycle du GBL s'effectue généralement en milieu basique par exemple en présence de soude caustique.
La réaction se produit par attaque nucléophile de l'ion hydroxyde (OH-) sur le carbone portant la fonction ester interne (lactone), celui-ci étant déficitaire en électrons par l'effet inductif attracteur de l'oxygène. Le cycle s'ouvre (lactonolyse) par retour d'un doublet d'électrons sur l'oxygène. On obtient ainsi le gamma-hydroxybutyrate. Une réaction de saponification peut en découler et conduire à la formation de gamma-hydroxybutyrate de sodium (sel sodique de l'acide gamma-hydroxybutyrique).
A noter : en milieu acide ou fortement anhydre, le GHB peut être reconverti dans sa forme lactone, donc en GBL.
Voir aussi
Articles connexes
Notes et références
- ↑ a , b , c , d , e , f , g , h et i gamma - BUTYROLACTONE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme » sur http://monographs.iarc.fr, 16 janvier 2009, CIRC. Consulté le 22 août 2009
- ↑ INRS - Fiche Toxicologique n°247 - Gamma Butyrolactone
- ↑ Les syndromes d'addiction et de manque sous GHB (et GBL) - projectghb.org
- Portail de la chimie
- Portail de la pharmacie
Catégories : Sédatif | Dépresseur | Butyrolactone | Arôme
Wikimedia Foundation. 2010.