- 75-47-8
-
Iodoforme
Iodoforme 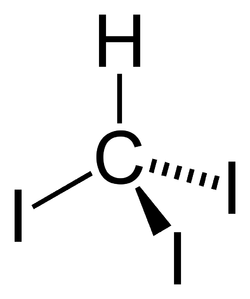
Général Nom IUPAC Triiodométhane No CAS No EINECS Apparence cristaux jaunâtres Propriétés chimiques Formule brute CHI3 [Isomères] Masse molaire 393,7321 g∙mol-1
C 3,05 %, H 0,26 %, I 96,69 %,Propriétés physiques T° fusion 123 °C T° ébullition 217 °C (explose) Solubilité 0,1 g/L (eau,20 °C) Masse volumique 4,008 g/cm³ Point d’éclair 204 °C Précautions Directive 67/548/EEC 
Xn
NPhrases R : 20/21/22, 36/37/38, Phrases S : 22, 26, 36/37/39, SIMDUT[1] 
Unités du SI & CNTP, sauf indication contraire. L’iodoforme ou triiodométhane était autrefois l’antiseptique par excellence et c’est cette odeur qui caractérisait les cabinets médicaux.
Les molécules qui renferment le groupe CH3-CO- ou CH3-CHOH- donnent, lorsqu’elles sont traitées par une solution alcaline de potassium iodé, un précipité jaune d’iodoforme (CHI3), dont l’odeur spéciale (un peu safranée) est caractéristique et tenace.
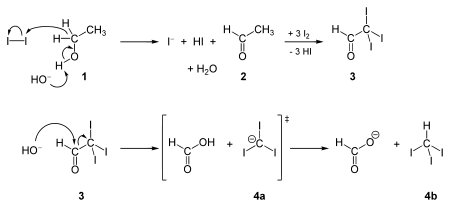
Synthèse
Le premier rapport de préparation de l'iodoforme date de 1822 par Georges Serullas, et sa formule moléculaire a été identifiée par Jean-Baptiste Dumas en 1834. Elle a été synthétisée par réaction haloforme, réaction du diiode en milieu basique sur un des quatre types de composés suivants:
- une méthylcétone: CH3COR, où R est une chaîne organique,
- l'acétaldéhyde (CH3CHO),
- l'éthanol (CH3CH2OH),
- et certains alcools secondaires, oxydables en méthylcétone (CH3CHROH, où R est un groupement alkyl ou aryl).
Cette réaction, appelée « test iodoforme », est utilisé pour la détection de méthylcétone par apparition d'un précipité jaune.
Références
- (en) Cet article est partiellement ou en totalité issu d’une traduction de l’article de Wikipédia en anglais intitulé « Iodoform ».
- Portail de la chimie
- Portail de la pharmacie
Catégories : Composé de l'iode | Produit chimique nocif | Produit chimique dangereux pour l'environnement | Halogénométhane | Iodoalcane | Antiseptique
Wikimedia Foundation. 2010.