- États de la matière
-
Phase (matière)
 Pour les articles homonymes, voir Phase.
Pour les articles homonymes, voir Phase.En sciences physiques, une phase est un milieu dans lequel les paramètres varient de manière continue ; cela inclut notamment la composition chimique et la densité. De fait, un corps pur dans un état donné (solide, liquide ou gazeux) constitue en général une seule phase.
Sommaire
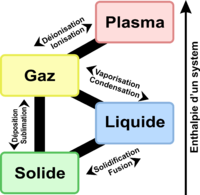
États de la matière
Voici une liste des 4 états de la matière :
- l'état gazeux ;
- l'état liquide ;
- l'état solide ;
- la mésophase ou cristal liquide, une phase intermédiaire entre liquide et solide.
Les pseudo-états suivants dérivent des précédents états :
- le condensat de Bose-Einstein (condensation de bosons dans le niveau de plus basse énergie), par exemple : le superfluide ou le condensat de rubidium (voir refroidissement d'atomes par laser) ;
- l'état plasma (ionisation d'un gaz) ;
- l'état supercritique (équilibre liquide-gaz obtenu par augmentation de la pression) ;
L'existence d'un état supersolide est controversée.
Définition générale
Bien que le concept de phase soit simple, il est difficile de le définir précisément. Une bonne définition de la phase d'un système est « une région de l'espace des paramètres thermodynamiques du système dans lequel l'énergie libre est une fonction analytique ». Ceci signifie que deux états d'un système sont dans la même phase s'il existe une transformation physique passant de l'un à l'autre sans qu'il y ait de changements abrupts dans les propriétés thermodynamiques.
Considérons un corps pur. Selon la pression et la température, ce corps pur peut être gazeux, liquide ou solide (voir état de la matière). S'il est solide, il peut cristalliser de différentes manières selon la pression et la température. Par exemple, le fer peut cristalliser sous forme cubique centrée (fer α) ou cubique à faces centrées (fer γ). Un solide peut aussi être amorphe. Par exemple, la silice SiO2 peut être cristalline (quartz, cristobalite) ou amorphe (verre de silice).
Ces différentes formes que peut prendre un corps pur (gaz, liquide, solide amorphe, solide cristallin de tel ou tel type) sont appelées phases. À l'équilibre, un corps pur ne peut être que dans une phase donnée.
Si l'on a un composé qui est un mélange de corps purs, on peut avoir, pour certaines conditions de pression et de température, plusieurs phases qui cohabitent. Par exemple, on peut avoir un mélange de deux poudres (deux phases solides différentes), un mélange liquide-gaz (aérosol), un mélange liquide-liquide (émulsion)...
On peut tracer une « carte » des phases, c'est-à-dire la phase dans laquelle est le système pour des conditions (pression, température, composition). Une telle carte est appelée diagramme de phase.
Il peut y avoir une phase homogène constituée de plusieurs corps purs (par exemple une solution aqueuse ou un eutectique), et un corps pur hors équilibre composé de plusieurs phases (par exemple un mélange eau-glace), la notion de phase est donc distincte de celle de composé chimique.
Toutes les propriétés thermodynamiques d'un système — l'entropie, la capacité thermique, la magnétisation, la compressibilité… — peuvent être exprimées en fonction de l'énergie libre et de ses dérivées. Par exemple, l'entropie peut s'exprimer simplement en fonction de la dérivée première de l'énergie libre par la température.
Une phase est parfois appelée « état de la matière », mais cette notion peut être confondue avec l'état thermodynamique. Par exemple, deux gaz maintenus à des pressions différentes sont dans des états thermodynamiques différents mais sont dans le même « état de matière ».
Définition thermodynamique
Les états de la matière se définissent fondamentalement d'un point de vue thermodynamique et correspondent à des niveaux d'agitation moléculaire. Le diagramme de phase représente les conditions de température et de pression pour passer d'un état à un autre. Lorsqu'un corps pur se retrouve dans les conditions, mesurées par le couple température-pression, qui ne correspondent à aucun point de l'une des courbes solide-liquide, liquide-gaz ou solide-gaz, alors ce corps est dans un état (solide, liquide ou gazeux) tel que la variation d'enthalpie entraîne directement une variation de température. En revanche, si le couple température-pression correspond à un point de l'une des courbes de changement de phase, la variation d'enthalpie n'entraîne pas de variation de température, c'est-à-dire que les changements de phase se font à température constante. Dans ce cas, un apport d'énergie provoqué par une variation positive d'enthalpie est convertie en chaleur latente, et une variation négative libère cette chaleur latente.
Définition physique
En physique, un état de la matière correspond à un certain degré de cohérence de la matière (densité, structure cristalline, indice de réfraction ...) qui se traduit par des comportements définis par les lois de la physique (malléabilité, ductilité, écoulement des fluides, loi des gaz parfaits ...). Mais les comportements de la matière ne sont pas toujours uniformes au sein d'un même état. Ainsi existe-t-il des états intermédiaires où l'on observe un solide se comporter comme un fluide (matière pulvérulente ou granuleuse) ou au contraire un liquide avoir certaines propriétés propres aux solides (émulsions).
Il existe par ailleurs des états exotiques de la matière tel que le plasma, le condensat de Bose-Einstein ou encore l'état supercritique qui nous sont moins familiers.
Il arrive également qu'on trouve la matière dans un état hors équilibre thermodynamique, les propriétés du matériau dépendent alors au cours du temps car celui ci se relaxe, sans jamais atteindre l'équilibre thermodynamique. Tout matériau spatialement hétérogène va rentrer dans cette définition dans la mesure où ces hétérogénéités spatiales vont se traduire par des contraintes internes impliquant ainsi un état non stable thermodynamiquement. Néanmoins, les temps de relaxation de tels systèmes peuvent atteindre des durées tellement longues qu'ils sont inobservable expérimentalement (allant jusqu'à plusieurs dizaines de milliers d'années).
Parmi ces matériaux on trouve de nombreux systèmes de la matière molle, ni solide, ni liquide tels que les verres, les gels ou bien les pâtes. Il n'est plus alors possible de parler de diagramme de phase (faisant référence à un état de la matière thermodynamiquement stable), le terme employé alors étant celui de diagramme d'état. Des diagrammes d'état unifiant les comportements des systèmes encombrés ont été établis pour de nombreux systèmes avec des interactions de type répulsif (granulaire, verres avec interaction de type volume exclu...) par Liu et Nagel en 1998, ainsi que pour les systèmes avec interaction de type attractif par Trappe, Prasad, Cipelletti, Segre, et Weitz, en 2001.
Voir aussi
- Portail de la chimie
- Portail de la physique
Catégories : Phase | Chimie générale
Wikimedia Foundation. 2010.