- Triméthylarsine
-
Triméthylarsine 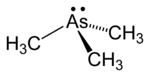
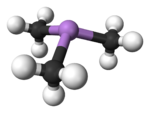
Squelette et représentation 3D Général No CAS No EINECS SMILES InChI Apparence liquide incolore Propriétés chimiques Formule brute C3H9As [Isomères] Masse molaire[1] 120,0252 ± 0,0031 g·mol-1
C 30,02 %, H 7,56 %, As 62,42 %,Propriétés physiques T° fusion -87,3 °C T° ébullition 52 °C Masse volumique 1,124 g·cm-3 Précautions Directive 67/548/EEC 
T
NPhrases R : 23/25, 50/53, Phrases S : 1/2, 20/21, 28, 45, 60, 61, Écotoxicologie DL50 7,870 mg·kg-1 (souris, oral)
90 mg·kg-1 (souris, intraveineuse)CL50 6,000 mg·m-3 (mammifères)
20,500 ppm en 4h (souris)Unités du SI & CNTP, sauf indication contraire. Le triméthylarsine est un composé chimique de formule chimique (CH3)3As, communément abrégée en AsMe3.
C'est un dérivé organique de l’arsine (AsH3), découvert[2] en 1854 mais ce n’est qu’en 1893 que le chimiste Italien Bartoloméo Gosio a publié les résultats de ses travaux sur le gaz toxique dit « Gaz Gosio », (Gaz qui s’est ensuite avéré être du triméthylarsine).Il est notamment utilisé comme source d’arsenic par l’industrie de la microélectroniques,
Sommaire
Caractéristiques chimiques
C'est un liquide incolore, toxique, de masse molaire 120,02 g/mol, de n°CAS , légèrement soluble dans l’eau, soluble dans divers solvants organiques.
- Point de fusion : -87,3 °C
- Point d’ébullition : 51 °C
- Point d’explosion : 100 °C
- Composés :
- acide cacodylique
- Triphénylarsine
Préparation
Il est produit à partir de trioxide d’arsenic, en réaction avec le Triméthylaluminium :
- As2O3 + 3 AlMe3 → 2 AsMe3 + Me-(Al-O)n
Réactivité
Le Triméthylarsine peut s'enflammer en raison d'une réaction exothermique des réactions suivantes :
- AsMe3 + 1/2 O2 → OAsMe3 (TMAO)
Sécurité/toxicité
Comme tous les composes organoarséniés, outre son caractère toxique immédiat, il est considéré comme cancérigène.
Voir aussi
- Arsenic
- Maladie de Haff
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- Source : Wikipédia anglais
- Wells, A.F., Structural Inorganic Chemistry (5e édition, Ed : Oxford University Press, 1984, ISBN 0198553706)
- Andrewes, Paul, et al., « Dimethylarsine and Trimethylarsine Are Potent Genotoxins In Vitro », dans Chem. Res. Toxicol., 16 (8), 994 -1003, 2003., 2003
- Irvin, T.Rick, et al., « In-vitro Prenatal Toxicity of Trimethylarsine, Trimethylarsine Oxide and Trimethylarsine Sulfide », dans Applied Organometallic Chemistry. vol. 9.315-321, 1995
- Sokolovskii, A.E., « Thermal Decomposition of Trimethylarsine », dans Kinetics and Catalysis, Vol 42, No. 6, 2001, pp. 743-745., 2001
- Hoshino, Masataka, « A mass spectrometric study of the decomposition of trimethylarsine (TMAs) with triethylgallium (TEGa) », dans Journal of Crystal Growth 110(1991)704-712, 1991
Liens externes
- Arsenic et santé résumé de GreenFacts d'un rapport scientifique du Programme International sur la Sécurité Chimique de l'OMS (fr)
- Document canadien sur l'arsenic (fr)
- Arsenic en milieu marin (dossier de 65p, fait par Ifremer, en 1993)(fr)
- Index by Molecular Formula en
- Information on Hazardous Chemicals by Class en
- "Highly efficient synthesis of trimethylarsine" E E Gavrilenko, L. A. ChekulaePa,* and L E Pisareva en
- Microbial Methylation of Metalloids: Arsenic, Antimony, and Bismuth en
- Arsenic Curiosa and Humanity en
- [1]
Catégories :- Composé de l'arsenic
- Produit chimique toxique
- Produit chimique dangereux pour l'environnement
- Cancérogène chimique
- Composé organo-arsénié
Wikimedia Foundation. 2010.
