- Acide cacodylique
-
Acide cacodylique 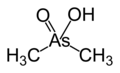
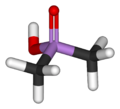
Formule semi-développée et représentation 3D de l'acide cacodylique Général Nom IUPAC acide dimethylarsinic Synonymes acide diméthylarsenic,
oxyde hydroxydiméthylarsine, asecodile,
ansar, silvisar,
Phytar 560, DMAA, UN 1572No CAS No EINECS No RTECS PubChem ChEBI SMILES InChI Apparence poudre ou cristaux blancs à incolore Propriétés chimiques Formule brute C2H7AsO2 [Isomères] Masse molaire[1] 137,9974 ± 0,0027 g·mol-1
C 17,41 %, H 5,11 %, As 54,29 %, O 23,19 %,pKa 6,15 Propriétés physiques T° fusion 192 à 198 °C T° ébullition 253,1 °C Solubilité 667 g·l-1 Masse volumique > 1,1 g·cm-3 Point d’éclair 109,4 °C Précautions Directive 67/548/EEC 
T
NPhrases R : 23/25, 50/53, Phrases S : 20/21, 28, 45, 60, 61, Transport 80 1572 Unités du SI & CNTP, sauf indication contraire. L'acide cacodylique est un composé chimique de formule (CH3)2AsO2H. Les dérivés de l'acide cacodylique, les cacodylates, sont fréquemment utilisés comme herbicides. Par exemple, l'« agent bleu », un des défoliants utilisés durant la Guerre du Viêt Nam, était un mélange d'acide cacodylique et de cacodylate de sodium.
Le cacodylate de sodium est couramment utilisé comme agent tampon dans la préparation et la fixation d'échantillons biologiques pour la microscopie électronique à transmission.Sommaire
Histoire
Les récentes recherches faites sur les cacodyles ont été effectuées par R. W. Bunsen à l'université de Marburg. Bunsen disait que « l'odeur de ce corps provoque des picotements instantanés dans les mains et les pieds, et même des vertiges et une insensibilité ». Il ajoutait : « On peut aussi noter que lorsqu'une personne est exposée à l'odeur de ces composés, la langue se couvre d'une substance noire, même quand aucun symptôme n'est notable ». Son travail a permis de mieux comprendre les radicaux méthylés.
Le cacodyloxyde, ((CH3)2As)2O, est souvent considéré comme le premier composé organométallique de synthèse.
Synthèse et réactions
Dans les années 1700, il était connu que la combinaison entre As2O3 et quatre molécules d'acétate de potassium (CH3CO2K) donnait un produit appelé « liquide fumant de Cadet » contenant de l'oxyde de cacodyle, ((CH3)2As)2O et du cacodyle, ((CH3)2As).
L'acide cacodylique peut être réduit en dérivés de diméthylarsine (III), intermédiaire utilisé dans la synthèse d'autres composés organoarséniques[2],[3] :
- (CH3)2AsO2H + 2 Zn + 4 HCl → (CH3)2AsH + 2 ZnCl2 + 2 H2O
- (CH3)2AsO2H + SO2 + HI → (CH3)2AsI + SO3 + H2O
Effets sur la santé
L'acide cacodylique est hautement toxique par ingestion, inhalation ou par contact avec la peau. Bien qu'il ait été considéré comme un sous-produit de la détoxification d'arsenic inorganique, on estime maintenant qu'il induit de sérieuses conséquences sur la santé. Il a été montré un effet tératogène chez les rongeurs, causant le plus souvent une fente palatine, mais aussi des morts fœtales à des doses élevées. De plus, il est génotoxique pour les cellules humaines, causant apoptose, diminution de la production d'ADN et raccourcissement des brins d'ADN. Bien que n'étant pas lui-même une substance cancérigène, l'acide cacodylique provoque des tumeurs en présence de carcinogènes au niveau de certains organes tels les reins ou le foie.
Voir aussi
- Arsenic
- Trihydrure d'arsenic (arsine)
- Cacodyle, Oxyde de cacodyle
Références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- Feltham, R. D.; Kasenally, A. and Nyholm, R. S., "A New Synthesis of Di- and Tri-Tertiary Arsines", Journal of Organometallic Chemistry, 1967, volume 7, 285-288.
- Burrows, G. J. and Turner, E. E., "A New Type of Compound containing Arsenic", Journal of the Chemical Society Transactions, 1920, 1374-1383
- Kenyon, E. M.; Hughes, M. F. "A Concise Review of the Toxicity and Carcinogenicity of Dimethylarsenic Acid." Toxicology 160 (2001): 227-236.
- Elschenbroich, C; Salzer, A. (1992) Organometallics, 2nd Edition
- Bunsen Biography
Liens externes
Wikimedia Foundation. 2010.

