Trifluorure d'antimoine
- Trifluorure d'antimoine
-
| Trifluorure d'antimoine |
|
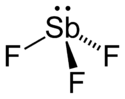 
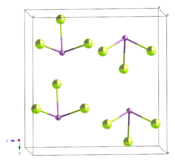
Molécule et cristal de trifluorure d'antimoine. |
| Général |
| Nom IUPAC |
Trifluorure d'antimoine |
| Synonymes |
Fluorure d'antimoine(III)
Réactif de Swart |
| No CAS |
7783-56-4 |
| No EINECS |
232-009-2 |
| PubChem |
10176366 |
| SMILES |
|
| InChI |
InChI : Vue 3D
InChI= 1S/ 3FH. Sb/ h3* 1H;/ q;;;+ 3/ p- 3
|
| Apparence |
solide cristallin blanc à incolore |
| Propriétés chimiques |
| Formule brute |
F3Sb
|
| Masse molaire[1] |
178,755 ± 0,001 g·mol-1
F 31,88 %, Sb 68,12 %,
|
| Propriétés physiques |
| T° fusion |
292 °C[2] |
| T° ébullition |
376 °C[2] |
| Solubilité |
4 430 g·l-1 (20 °C, eau)
5 620 g·l-1 (30 °C, eau)[2] |
| Masse volumique |
4,379 kg·m-3 (solide, 20,9 °C[2] |
| T° d'auto-inflammation |
Ininflammable |
| Pression de vapeur saturante |
263,4 mbar à 292 °C |
| Précautions |
|
Directive 67/548/EEC
|

T
|

N
|
|
Symboles :
T : Toxique
N : Dangereux pour l’environnement
Phrases R :
R23/24/25 : Toxique par inhalation, par contact avec la peau et par ingestion.
R51/53 : Toxique pour les organismes aquatiques, peut entraîner des effets néfastes à long terme pour l’ environnement aquatique.
Phrases S :
S7 : Conserver le récipient bien fermé.
S26 : En cas de contact avec les yeux, laver immédiatement et abondamment avec de l’ eau et consulter un spécialiste.
S45 : En cas d’ accident ou de malaise, consulter immédiatement un médecin ( si possible, lui montrer l’ étiquette).
S61 : Éviter le rejet dans l’ environnement. Consulter les instructions spéciales/ la fiche de données de sécurité.
|
| Phrases R : 23/24/25, 51/53, |
| Phrases S : 7, 26, 45, 61, |
|
Transport
|
Code Kemler :
60 : matière toxique ou présentant un degré mineur de toxicité
Numéro ONU :
1549 : COMPOSÉ INORGANIQUE SOLIDE DE L’ ANTIMOINE, N. S. A. à l’ exception des sulfures et des oxydes d’ antimoine contenant au plus 0, 5 pour cent ( masse) d’ arsenic
Classe :
6. 1
Étiquette :
 6.1 : Matières toxiques
6.1 : Matières toxiques
|
|
Unités du SI & CNTP, sauf indication contraire.
|
Le trifluorure d'antimoine, aussi appelé réactif de Swart, est un composé chimique de formule SbF3. A température ambiante, il se présente sous la forme d'un solide cristallin gris clair utilisé comme pigment et dans les céramiques.
Synthèse
Le trifluorure d'antimoine peut être synthétisé à partir de fluorure d'hydrogène avec le trioxyde d'antimoine[3].

Notes et références
- ↑ Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- ↑ a, b, c et d Entrée du numéro CAS « 7783-56-4 » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 05/07/09 (JavaScript nécessaire)
- ↑ Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (2nd ed.), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4
Catégories : - Composé de l'antimoine
- Produit chimique toxique
- Produit chimique dangereux pour l'environnement
- Fluorure
Wikimedia Foundation.
2010.
Contenu soumis à la licence CC-BY-SA. Source : Article Trifluorure d'antimoine de Wikipédia en français (auteurs)
Regardez d'autres dictionnaires:
Trifluorure d'azote — Général … Wikipédia en Français
Pentafluorure d'antimoine — Structure … Wikipédia en Français
7783-56-4 — Trifluorure d antimoine Trifluorométhane … Wikipédia en Français
Liste de composés inorganiques S — Sommaire 1 Soufre 2 Antimoine 3 Scandium 4 Sélénium 5 … Wikipédia en Français
Liste des composés inorganiques S — Liste de composés inorganiques S Sommaire 1 Soufre 2 Antimoine 3 Scandium 4 Sélénium … Wikipédia en Français
HALOGÉNÉS (DÉRIVÉS) — Les dérivés halogénés résultent du remplacement, par des halogènes F, Cl, Br, I, d’un ou de plusieurs atomes d’hydrogène des hydrocarbures. Ils se rencontrent rarement à l’état naturel: présence d’iode dans la tyroxine, présence de chlore dans… … Encyclopédie Universelle
75-46-7 — Trifluorométhane Trifluorométhane Général Nom … Wikipédia en Français
Fluoroforme — Trifluorométhane Trifluorométhane Général Nom … Wikipédia en Français
HFC-23 — Trifluorométhane Trifluorométhane Général Nom IU … Wikipédia en Français
Trifluorométhane — Général Nom IUPAC … Wikipédia en Français







