- Polyacétate de vinyle
-
Polyacétate de vinyle 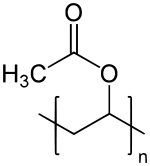
Général No CAS SMILES Propriétés chimiques Formule brute (C4H6O2)n Masse molaire[1] 86,0892 ± 0,0042 g·mol-1
C 55,81 %, H 7,02 %, O 37,17 %,Propriétés physiques T° transition vitreuse 30 °C[2] Propriétés électroniques constante diélectrique 3,5 (1 MHz, 50 °C)
8,3 (1 MHz, 150 °C)[3]Propriétés optiques Indice de réfraction  1,46–1,47 [4]
1,46–1,47 [4]Précautions Classification du CIRC Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[5] Unités du SI & CNTP, sauf indication contraire. Le polyacétate de vinyle, ou acétate de polyvinyle, abrégé en PVAc (mais parfois aussi PVA, à ne pas confondre avec le PVA désignant l'alcool polyvinylique) est un polymère synthétique. Il est synthétisé par polymérisation de l'acétate de vinyle. L'hydrolyse complète ou partielle de ce polymère permet de fabriquer l'alcool polyvinylique; il s'agit d'une saponification. Cette réaction a été découverte par le chimiste allemand Fritz Klatte en 1912.
Sommaire
Utilisations
- Le PVAc est vendu en guise de colle sous forme d'émulsion dans de l'eau. Il s'agit de la "colle blanche" particulièrement efficace sur les matériaux poreux comme le bois, le papier ou le tissu. Ainsi, la colle PVAc est utilisée notamment dans la fabrication de livres (pour sa flexibilité et son caractère non-acide contrairement à beaucoup de polymères).
- Aux États-Unis, une des marques de colle les plus populaires, Elmer's Glue est composée de PVAc.
- On emploie également le polyacétate de vinyle pour fabriquer des copolymères plus coûteux avec des acrylates. Ils sont exploités dans la chimie du papier, des peintures et celle des revêtements industriels.
- Il est utilisé également pour protéger les fromages des moisissures et de l'humidité.
- Il est attaqué par l'alcali, qui lui fait subir une hydrolyse aboutissant à la formation d'acide acétique.
- Les composés borés comme l'acide borique ou le borax entraînent la réticulation du PVAc qui forme alors une pâte comparable au Silly Putty.
- Enfin, le PVAc est couramment utilisé pour fabriquer du papier-mâché.
Voir aussi
Liens internes
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- (en) Charles E. Wilkes, James W. Summers, Charles Anthony Daniels, Mark T. Berard, PVC Handbook, Munich, Hanser Verlag, 2005, 1re éd. (ISBN 978-1-56990-379-7) (LCCN 2005013540) [lire en ligne]
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, 2009, 90e éd., Relié, 2804 p. (ISBN 978-1-420-09084-0)
- (en) J. G. Speight, Norbert Adolph Lange, Lange's handbook of chemistry, McGraw-Hill, 2005, 16e éd., 1623 p. (ISBN 0071432205), p. 2.807
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme » sur http://monographs.iarc.fr, CIRC, 16 janvier 2009. Consulté le 22 août 2009
Wikimedia Foundation. 2010.
