- Kligler
-
Kligler-Hajna
Le milieu de Kligler-Hajna est un milieu permettant la recherche simultanée de :
- L'utilisation du lactose ;
- La fermentation du glucose ;
- La production d'H2S ;
- La production de gaz ;
- La lysine décarboxylase.
- La B-galactosidase pour les bactéries lactose - (test ONPG).
Sommaire
Composition
- Peptone ......................... 15 g - Extrait de viande ............... 3 g - Extrait de levure ............... 3 g - Peptone pepsique de viande ...... 5 g - Glucose ......................... 1 g - Lactose ......................... 10 g - Rouge de phénol ................. 25 mg - Chlorure de sodium .............. 5 g - Sulfate ferreux.............. 0,2 g - Thiosulfate de sodium ........... 0,3 g - Agar-agar ....................... 11 g
pH = 7,5
Les peptones sont riches en lysine. Le milieu est conditionné en tubes avec une pente et un culot.
Ensemencement
- La pente doit être abondamment ensemencée (stries serrées).
- Le culot est ensemencé simple piqûre.
Incubation : 37 °C pendant 18 à 24 h (ne pas dépasser ce délai) après avoir dévisser le bouchon partiellement ce qui permet les échanges gazeux.
Lecture, interprétation
Utilisation des glucides
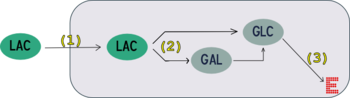
Pour pouvoir utiliser le lactose, une bactérie doit posséder deux enzymes (schéma ci-contre) :
- Une β-galactoside perméase (1) ;
- Une β-galactosidase (2) .
Il s'en suit une série de réactions de dégradation du glucose (3) conduisant à la production d'énergie E.
Le glucose inhibe la synthèse de ces deux enzymes. C'est ce que l'on appelle l'effet glucose. En effet, l'utilisation des glucides suit la loi de diauxie, l'utilisation du lactose n'aura lieu qu'après épuisement du glucose. Or, le glucose est en faible quantité par rapport au lactose et la pente est ensemencée abondamment.
La pente et le culot doivent être interprétés indépendamment.
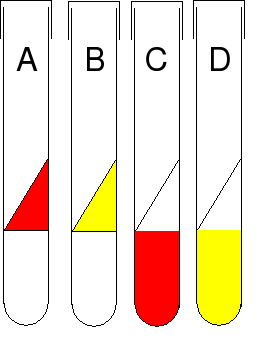 Figure 1 : Résultats de l'incubation du milieu de Kligler-Hajna.
Figure 1 : Résultats de l'incubation du milieu de Kligler-Hajna.Interprétation de la pente
- Dans un premier temps, les bactéries utilisent le glucose comme source de carbone et d'énergie (à cause de l'effet glucose). Cette utilisation s'accompagne de la production d'acides organiques d'où le virage du rouge au jaune du milieu (figure 1A).
- Dans un second temps, du fait du développement rapide (en aérobiose) et de la faible concentration en glucose en moins de 24 heures, la totalité du glucose est dégradé, il y a disparition de l'effet glucose. Puis, deux possibilités :
- Si la bactérie est β-galactoside perméase + ET β-galactosidase + : les bactéries utilisent le lactose avec production d'acides organiques : le virage au jaune est confirmé (figure 1B).
- Si la bactérie est β-galactoside perméase + et β-galactosidase - OU β-galactoside perméase - et β-galactosidase - : les bactéries ne peuvent pas utiliser le lactose. Les bactéries utilisent alors comme source de carbone et d'énergie les peptones (qui ne sont dégradables qu'en conditions aérobies) : le métabolisme protique libère des produits basiques (ammoniac, amines...) d'où une recoloration au rouge de la pente (figure 1).
Ainsi :
Interprétation du culot
- Dans un premier temps, les bactéries fermentent le glucose avec production importante d'acides organiques (à cause de l'effet glucose) (figure 1D).
- Comme sur la pente, en moins de 24 heures, tout le glucose est fermenté. Cependant, si les bactéries sont lactose -, l'utilisation des peptones avec une alcalinisation ne permet pas le revirage de l'indicateur de pH, le culot restera jaune en 24 h (figure 1D).
- Si la bactérie n'est pas capable de fermenter le glucose, il n'y a pas production d'acides organiques, le culot reste rouge (figure 1C).
Ainsi :
Production de gaz
La production de gaz lors de l'utilisation des glucides est mise en évidence par le décollement de la gélose et/ou des bulles dans la gélose.
elle est donc Gaz -
Production de sulfure d'hydrogène
Elle a lieu à partir de l'ion thiosulfate :
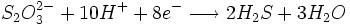 Le sulfure d'hydrogène réagit avec les ions fer III (Fe3+) du citrate de fer pour former un précipité de sulfure de fer noir. Ainsi :
Le sulfure d'hydrogène réagit avec les ions fer III (Fe3+) du citrate de fer pour former un précipité de sulfure de fer noir. Ainsi :- Bactéries H2S + : précipité noir ;
- Bactéries H2S - : pas de précipité noir ;
Présence d'une lysine décarboxylase
La lysine décarboxylase (LDC) décarboxyle la lysine présente dans le milieu en cadavérine (amine très apolaire en milieu basique) soluble dans le chloroforme. La ninhydrine permet de mettre en évidence la cadavérine.
- Verser 1 mL de potasse (1 mol/L) sur la pente du milieu de Kligler.
- Verser 1 mL de chloroforme et laisser décanter.
- Prélever la phase chloroformique (en bas) et verser dans un tube à hémolyse en verre.
- Ajouter quelques gouttes de ninhydrine (en solution chloroformique à 1 g/L) dans le tube à hémolyse.
- Incuber quelques minutes au bain-marie à 37 °C.
- Lecture :
Remarque : les acides aminés n'interfèrent pas sur la réaction car, en milieu basique, ils sont polaires donc insolubles dans un solvant apolaire comme le chloroforme.
Catégorie : Milieu de culture
Wikimedia Foundation. 2010.