- K2CO3
-
Carbonate de potassium
Carbonate de potassium 
Général Nom IUPAC Carbonate de potassium No CAS No EINECS No E E501(i) Apparence solide blanc Propriétés chimiques Formule brute K2CO3 Masse molaire 138,2055 g∙mol-1
C 8,69 %, K 56,58 %, O 34,73 %,Propriétés physiques T° fusion 891 °C T° ébullition décomposition Solubilité 1120 g/L dans l'eau Masse volumique 2,428 , solide Précautions SIMDUT[1] 
Unités du SI & CNTP, sauf indication contraire. Le carbonate de potassium, K2CO3, est un sel blanc hygroscopique.
Sommaire
Historique
Le carbonate de potassium a été identifié la première fois par Antonio Campella et est le composant principal de la potasse.
Propriétes
Le carbonate de potassium est très soluble dans l'eau (1 120 g/L) et donne des solutions basiques. Par hydrolyse, une solution de carbonate de potassium donne de l'hydroxyde de potassium : K2CO3 + H2O → KHCO3 + KOH.
Avec les acides, il se produit la formation de dioxyde de carbone et du sel de potassium correspondant.
Préparation
- Carbonatation de l'hydroxyde de potassium :
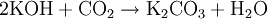 Cette réaction est la réaction qui est utilisée de nos jours pour préparer industriellement le carbonate de potassium. L'hydroxyde de potassium étant produit au préalable par électrolyse du chlorure de potassium.
Cette réaction est la réaction qui est utilisée de nos jours pour préparer industriellement le carbonate de potassium. L'hydroxyde de potassium étant produit au préalable par électrolyse du chlorure de potassium.- La réaction d'une solution d'hydroxyde de calcium avec du sulfate de potassium et du monoxyde de carbone sous 30 bar, le sel de potassium de l'acide méthanoïque obtenu est ensuite oxydé par calcination :
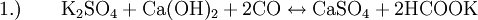
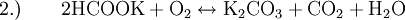 Cette réaction n'a plus d'intérêt industriel.
Cette réaction n'a plus d'intérêt industriel.- Le carbonate de potassium est un additif alimentaire portant le numéro E501(i).
Références
- ↑ « Carbonate de potassium » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009
- Portail de la chimie
Catégories : Composé du potassium | Produit chimique corrosif | Carbonate
Wikimedia Foundation. 2010.
