- 138-59-0
-
Acide shikimique
Acide shikimique 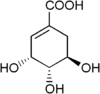
Structure de l'acide shikimique Général Nom IUPAC Acide (3R,4S,5R)-3,4,5-trihydroxy-
1-cyclohexènecarboxyliqueNo CAS No EINECS Propriétés chimiques Formule brute C7H10O5 [Isomères] Masse molaire 174,1513 g∙mol-1
C 48,28 %, H 5,79 %, O 45,94 %,Propriétés physiques T° fusion 185 à 187 °C Précautions Classification du CIRC Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[1] Unités du SI & CNTP, sauf indication contraire. L'acide shikimique, plus connu sous sa forme anionique, les shikimates, est un intermédiaire biochimique important dans les plantes et les micro organismes. Il doit son nom à la fleur japonaise shikimi (シキミ, Illicium anisatum ou badiane japonaise), d'où il a été isolé.
L'acide shikimique est présent dans la plupart des organismes autotrophes, mais le rendement d'isolation est bas. L'acide shikimique extrait de l'anis étoilé chinois est à la base de la fabrication de l'oseltamivir ou "Tamiflu", chimiothérapie antigrippale non-vaccinale.
L'acide shikimique est le précurseur :
- de la phénylalanine et de la tyrosine, des acides aminés aromatiques ;
- de l'indole, des dérivés de l'indole et du tryptophane ;
- de nombreux alcaloïdes et d'autres métabolites aromatiques ;
- des tanins;
- de la lignine.
- de l'acide salicylique
Également, la synthèse du shikimate est inhibée par une molécule herbicide : le glyphosate (nom commercial : Round up).
Son numéro EINECS est 205-334-2.
Biosynthèse
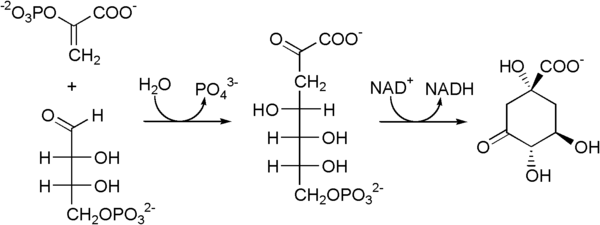
Le phosphoénol pyruvate et l'érythrose-4-phosphate réagissent entre eux pour former le 3-désoxy-2-céto-arabinoheptonate-7-phosphate. Celui-ci est alors oxydé par le NAD+ pour former du 3-déhydroquinate.
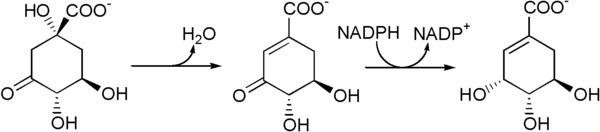
Le 3-déhydroquinate est déshydraté en 3-déhydroshikimate, lequel est réduit par le NADPH en shikimate.
Liens externes
Notes et références
- ↑ IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme » sur http://monographs.iarc.fr, 16 janvier 2009, CIRC. Consulté le 22 août 2009
- Portail de la biologie
- Portail de la chimie
Catégories : Acide carboxylique | Alcool (chimie)
Wikimedia Foundation. 2010.