- Effet Stérique
-
Effet stérique
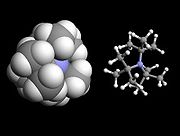
L'effet stérique d'une molécule de tri-(tert-butyl)amine rend les réactions electrophiles, comme la formation ici de cations de tetraalkylammonium, difficile. Il est difficile pour les électrophiles de se rapprocher et d'attaquer les doublets non liants de la molécule d'azote (ici en bleu).
L'effet stérique provient du fait que chaque atome contenu dans une molécule occupe un certain espace. Si certains atomes sont amenés trop près les uns des autres, il y a un cout énergétique associé à ce rapprochement. En effet, une certaine quantité d'énergie est requise pour chevaucher le nuage électronique (répulsion de Pauli ou de Born). Et ce cout énergétique affecte la forme normale de la molécule ainsi que ses propriétés lors d'une réaction chimique.
Sommaire
Les différents types d'effets stériques
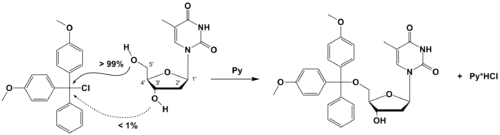
Article détaillé : Encombrement stérique.L'encombrement stérique ou gène stérique se produit lorsque le volume occupé par une partie d'une molécule gêne l'approche d'un réactif ou d'une autre partie de la molécule. Bien que l'encombrement stérique soit de temps en temps un problème, il peut être aussi un outil très utile. La résistance stérique est souvent employée par les chimistes pour modifier le comportement d'une molécule dans une réaction chimique, en stoppant toute réaction parasite (protection stérique). L'encombrement stérique entre deux groupes adjacents peut aussi restreindre l'angle de torsion. De plus, une hyperconjugaison a été suggérée comme explication de la conformation décalée de la molécule d'éthane, l'encombrement stérique de l'atome d'hydrogène étant bien trop petit.[1][2].
La répulsion stérique se produit lorsqu'un groupe chargé d'une molécule est apparemment affaibli ou spatialement protégé par des atomes moins chargés (ou de charge opposée), y compris les ions en solutions (répulsion de Debye). Dans certains cas, pour un atome interagissant avec des atomes bénéficiant d'une protection stérique, l'atome devra s'approcher à partir d'un voisinage moins protégé. Ceci permet de contrôler quand et dans quelle direction une interaction moléculaire va se réaliser.
L'attraction stérique se produit lorsque des molécules présentent des formes ou des géométries optimisées pour leurs interactions. Dans ce cas, les molécules vont réagir les unes avec les autres d'une façon, le plus souvent, spécifique.
Croisement de chaînes – Une pelote aléatoire ne peut pas changer, par un léger déplacement, d'une conformation à une autre forme relativement proche, si ce dernier requiert qu'un polymère passe à travers un autre, ou à travers lui-même.
Effet stérique contre effet électronique
La structure, les propriétés et la réactivité d'une molécule dépendent strictement des liaisons chimiques (et de leurs interactions), comme les liaisons covalentes, les liaisons ioniques, les liaisons hydrogènes et d'autres formes mineures de liaisons. Ces liaisons fournissent un squelette moléculaire basique, aisément modifiable par des forces répulsives. Ces forces comprennent les interactions stériques décrites plus haut. Les effets stériques et interactions basiques sont néanmoins toujours insuffisant pour expliquer beaucoup de structures, de propriétés et de réactions. Ainsi, les effets stériques sont souvent mis en opposition ou complétés par les effets électroniques, impliquant l'influence d'effets comme l'induction, la conjugaison, la symétrie moléculaire ou encore les interactions électrostatiques. D'autres effets électroniques obscurs existes, mais ces derniers sont les plus importants lorsque l'on considère la structure et la réactivité chimique.
Importance
Comprendre les effets stériques est crucial en chimie, biochimie et pharmacologie. En chimie, les effets stériques sont pratiquement universels et affectent, à différents degrés, la plupart des réactions chimiques. En biochimie, les effets stériques sont souvent utilisés dans les molécules naturelles comme les enzymes, là où le lieu de catalyse peut être caché dans une grande structure protéique. En pharmacologie, les effets stériques déterminent comment et à quel niveau un médicament agira avec ses bio-molécules cibles.
Voir aussi
Références
- (en) Cet article est partiellement ou en totalité issu d’une traduction de l’article de Wikipédia en anglais intitulé « Steric effects ».
- ↑ Hyperconjugation not steric repulsion leads to the staggered structure of ethane Pophristic, V. & Goodman, L. Nature 411, 565–568 (2001)Abstract DOI:10.1038/35079036
- ↑ Chemistry: A new twist on molecular shape Frank Weinhold Nature 411, 539-541 (31 May 2001) DOI:10.1038/35079225
- ↑ Michael Gait, Oligonucleotide synthesis: a practical approach, IRL Press, Oxford (ISBN 0904147746)
Liens externes
- (en) http://www.chem.swin.edu.au/modules/mod4/qsarwebp4.html
- (en) http://www.gh.wits.ac.za/craig/steric/
- (en) http://jilawww.colorado.edu/pubs/thesis/fair/
- Portail de la chimie
Catégorie : Liaison chimique
Wikimedia Foundation. 2010.