- 1,3-diméthylbenzène
-
Xylène
Le terme xylène se réfère à un groupe de trois dérivés du benzène, correspondant aux isomères ortho-, méta- et para- du diméthylbenzène. Le xylène technique est un mélange des trois isomères, de composition voisine de méta- (60%), ortho- (10-25%) et para- (10-25%).
Sommaire
Structure et isomères
Tout comme pour le benzène, la structure du xylène est plane. C'est un composé aromatique, et les électrons formant les liaisons π du cycle sont délocalisés, ce qui entraîne une stabilité importante de la structure.
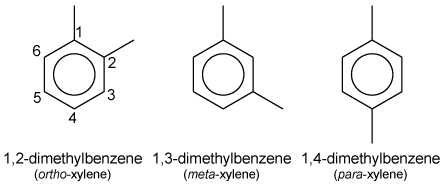
Le préfixe o- (xylène), p- ou m- indique à quels atomes de carbone du noyau aromatique sont fixés les groupements méthyles. Un numérotant les atomes de carbone à partir d'un atome lié à un groupement méthyle, le composé est du o-xylène (1,2-diméthylbenzène) si l'atome de carbone adjacent, numéroté 2, est également lié à un groupement méthyle. Si le carbone numéroté 3 est lié à un groupement méthyle, le composé est le m-xylène (1,3-diméthylbenzène). Si le carbone numéroté 4 est lié à un groupement méthyle, le composé est le p-xylène (1,4-diméthylbenzène).
Propriétés physico-chimiques
Le xylène est un liquide incolore, d'odeur agréable et très inflammable. Il est naturellement présent dans le pétrole et le goudron de houille, et se forme durant les feux de forêts. Les propriétés chimiques diffèrent peu d'un isomère à l'autre. La température de fusion est comprise entre (-47,87 °C (m-Xylène) et 13,26 °C (p-Xylène). La température d'ébullition est voisine de 140 °C pour tous les isomères. La densité est de 0,87 (le composé est plus léger que l'eau. L'odeur du xylène devient détectable pour des concentrations de l'ordre de 0,08 à 3,7 ppm, et le goût est apparent dans l'eau pour des concentrations de l'ordre de 0,53 à 1,8 ppm.
Isomères du xylène Général nom o-xylène m-xylène p-xylène nom complet 1,2-diméthylbenzène 1,3-diméthylbenzène 1,4-diméthylbenzène autres noms o-xylol m-xylol p-xylol Formule chimique C8H10 SMILES Cc1c(C)cccc1 Cc1cc(C)ccc1 Cc1ccc(C)cc1 Masse molaire 106.16 g/mol Apparence liquide incolore Numéro CAS Numéro CAS pour le mélanges des 3 isomères Propriétés Densité 0.88 g/cm³, liquide 0.86 g/cm³, liquide 0.86 g/cm³, liquide Solubilité dans l'eau quasiment insoluble Soluble dans les solvants non polaires comme les hydrocarbures aromatiques Température de fusion -25 °C (248 K) -48 °C (225 K) 13 °C (286 K) Température d'ébullition 144 °C (417 K) 139 °C (412 K) 138 °C (411 K) température d'auto-inflammation 463 °C (736 K) 527 °C (800 K) 528 °C (801 K) Pression de vapeur ~8 hPa à 20 °C Viscosité ? cP à 25 °C ? cP à 25 °C ? cP à 25 °C Sécurité Dangers inflammable, toxique par ingestion et inhalation, réagit avec les acides forts et les oxydants forts Point d'éclair 32 °C 27 °C 27 °C Phrases R et S R: 10 - 20/21 - 38 S: 2 - 25NFPA 704 SIMDUT (mélange d'isomères)[1] 

SIMDUT[2],[3],[4] 





SGH[5] 

AttentionDJA 1,5 mg/kg p.c./jour[6] Composés dérivés hydrocarbures aromatiques toluène, mésitylène, benzène, éthylbenzène Autres xylènols - analogue du phénol Sauf mentions contraires, les valeurs sont données
pour les composés à l'état standard (à 25 °C, 100 kPa)Production et utilisation
Le xylène est produit à partir du pétrole dans l'industrie pétrochimique. En termes de volume, c'est l'un des 30 composés chimiques les plus produits aux USA (environ 450 000 tonnes par an). Il est utilisé comme solvant, ainsi que par les industries de l'impression, du caoutchouc et du cuir. Il est employé comme réactif de départ pour la production d'acide téréphtalique, utilisé comme monomères pour la production de polymères de type téréphtalates. Le xylène est également utilisé pour le nettoyage, comme pesticide, Utilisé aussi dans la parasitologie dans le méthode de KOHN pour vérification la bonne déshydratation de frottis de selle, comme diluant pour la peinture ainsi que dans la peinture et les vernis. Il est présent en faibles quantités dans les carburants pour l'aviation ainsi que dans l'essence. En présence de réactifs oxydants, comme le permanganate de potassium KMnO4, le groupement méthyle peut être oxydé jusqu'à former un acide carboxylique. Lorsque les deux groupements méthyles sont oxydés, le o-xylène forme l'acide phtalique et le p-xylène l'acide téréphtalique.
Séparation des isomères
Les températures d'ébullition des trois isomères étant très proches, il n'est pas possible de les séparer par distillation. En revanche, les produits de sulfonation peuvent être séparé par distillation. Le o-xylène peut être séparé des deux autres isomères par rectification. Enfin, les températures de fusion étant suffisamment distinctes, il est possible d'effectuer une séparation des trois isomères par cristallisation fractionnée.
Effets sur la santé
Le xylène a un effet nocif sur le cerveau. Des niveaux d'expositions élevés pour des périodes même courtes peuvent entraîner des maux de tête, un défaut de coordination des muscles, des vertiges, la confusion et des pertes du sens de l'équilibre. Des expositions à des taux élevés pendant de courtes périodes de temps peuvent également occasionner une irritation de la peau, des yeux, du nez et de la gorge, des difficultés de respiration, des problèmes pulmonaires, une augmentation des temps de réaction, des pertes de mémoires, des irritations d'estomac et des altérations du fonctionnement du foie et des reins. Des taux d'exposition très élevés peuvent entraîner la perte de conscience voire la mort.
Des études sur des animaux ont montré que des concentrations de xylène élevées entraînent une augmentation du nombre d'animaux morts-nés, ainsi que des retards de croissance et de développement. Dans beaucoup de cas, ces mêmes concentrations ont également des effets négatifs sur la santé des mères. L'effet d'expositions de la mère à de faibles concentrations de xylène sur le fœtus n'est pas connu à l'heure actuelle.
Il est toutefois utilisé en médecine. Il entre dans la composition de gouttes auriculaires utilisées pour ramollir les bouchons de cérumen et faciliter leur expulsion par action mécanique ( Jet d'eau ).
Phrases de sécurité
- R: 10 (Inflammable)
- R: 20/21 (Nocif par inhalation et par contact avec la peau)
- R: 38 (Irritant pour la peau)
- S: 2 (Conserver hors de la portée des enfants)
- S: 25 (Éviter le contact avec les yeux)
Voir aussi
Références
- Bewertung von Toluol- und Xylol-Immissionen. Erich Schmidt Verlag, Berlin (2000), ISBN 3503040714 (allemand)
- ↑ « Xylène (mélange d'isomères) » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ « Xylène (ortho-) » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ « Xylène (meta-) » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ « Xylène (para-) » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- ↑ Concentrations/doses journalières admissibles et concentrations/doses tumorigènes des substances d'intérêt prioritaire calculées en fonction de critères sanitaires, publié par Santé Canada
Liens externes
- Portail de la chimie
Catégories : Hydrocarbure aromatique | Solvant
Wikimedia Foundation. 2010.





