- 79-01-6
-
Trichloréthylène
Trichloréthylène 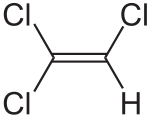
Général Synonymes 1,1,2-Trichloroéthylène
Trichloroéthène
Trichlorure d'acétylène
Trichlorure d'éthylèneNo CAS No EINECS PubChem SMILES InChI Apparence liquide incolore, d'odeur caractéristique.[1] Propriétés chimiques Formule brute C2HCl3 [Isomères] Masse molaire 131,388 g∙mol-1
C 18,28 %, H 0,77 %, Cl 80,95 %,Propriétés physiques T° fusion -73 °C[1] T° ébullition 87 °C[1] Solubilité dans l'eau à 20 °C : 0.1 g/100 ml[1] Masse volumique (eau = 1) : 1.5[1],
Vapeurs plus denses que l'airT° d’auto-inflammation 410 °C[1] Limites d’explosivité dans l’air en volume % dans l'air : 8-10.5[1] Pression de vapeur saturante à 20 °C : 7.8 kPa[1] Précautions Directive 67/548/EEC 
TPhrases R : 36/38, 45, 52/53, 67, Phrases S : 45, 53, 61, [2] Transport 60 1710 NFPA 704 SIMDUT[4] 
SGH[5] 
DangerClassification du CIRC Groupe 2A : Probablement cancérogène pour l'homme[3] Inhalation amener à l'air frais, éventuellement réanimation cardiopulmonaire Peau enlever les vêtements souillés, laver à grande eau, montrer à un médecin Yeux laver à grande eau en maintenant les paupières ouvertes, montrer à un ophtalmologiste Ingestion ne pas faire boire, ne pas faire vomir, contacter un médecin. Écotoxicologie LogP 2.42[1] Unités du SI & CNTP, sauf indication contraire. Le trichloréthylène (ou trichloroéthylène) est un composé organique de formule brute C2HCl3 et de formule semi-développée ClCH=CCl2.
Il est également appelé trichloréthène (ou trichloroéthène), trichlorure d'éthylène ou d'éthène, trilène ou tout simplement trichlo ou trichlore.
Il s'agit d'une molécule d'éthène dont trois atomes d'hydrogène ont été remplacés par des atomes de chlore.
Sommaire
Dangers et précautions d'emploi
En 1995, le trichloréthylène a été classé « carcinogène[6] probable » (il était auparavant classé « carcinogène possible ») par l'International Agency for Research on Cancer (IARC). Ceci a été entériné par la directive européenne 2001/59/CE de la Commission du 6 août 2001 portant vingt-huitième adaptation au progrès technique de la directive 67/548/CEE.
Il irrite la peau et les muqueuses, et est un toxique pour le système nerveux central : inhalé à de fortes teneurs (au-delà de 3 000 ppm), il peut entraîner le coma voire la mort en quelques minutes. De nombreux cas de maladie professionnelle ont été rapportés suite à une manipulation prolongée.
En présence de flamme ou a une température supérieure à 120 °C il peut se décomposer en :
- monoxyde de carbone CO,
- chlorure d'hydrogène HCl,
- dichlore Cl2
trois gaz extrêmement toxiques.
S'il est lui-même non combustible, en revanche, ses vapeurs peuvent être explosives si elles se mélangent avec l'air (elles sont plus lourdes que l'air).
L'eau ainsi que certains métaux (Aluminium) provoquent la décomposition du Trichloréthylène avec production d'acide chlorhydrique. L'acide chlorydrique peut être neutralisé par ajout de stabilisants.
Il doit être stocké dans un endroit bien ventilé, avec une température comprise entre 15 °C et 25 °C. Il doit être manipulé en milieu bien ventilé, avec des gants et des lunettes de protection. l'INRS préconise l'utilisation de gants en PVA (alcool polyvinylique). En cas d'exposition accidentelle de la peau et des muqueuses, il faut enlever les vêtements souillés, laver abondamment à l'eau et consulter un médecin.
Selon la réglementation européenne, son utilisation est interdite pour les particuliers à une concentration supérieure à 0,1 %. Dans l'industrie, il faut procéder si possible à son remplacement par d'autres produits comme le tétrachloroéthylène (ou perchloroéthylène), le chlorure de méthylène (ou dichlorométhane (DCM)), d'autres dérivés d'’hydrocarbures (cétones, alcools,…), ou par certains fluoroalcanes.
Utilisation
Les deux principales caractéristiques intéressantes du trichloréthylène sont :
- qu'il s'agit d'un solvant ;
- que contrairement à la plupart des solvants, il est peu inflammable.
Il a beaucoup été utilisé pour le dégraissage de pièces métalliques, le nettoyage à sec de vêtements et l'extraction de produits organiques. Il fut utilisé comme anesthésiant sous le nom trilène.
Il tend à être progressivement remplacé par des produits moins dangereux, et est d'ores et déjà interdit pour les particuliers dans l'Union européenne.
Le trichloréthylène passe en catégorie 2 des substances cancérogènes (Directive de l'Union Européenne sur les substances dangereuses) avec la phrase de risque R45 "peut causer le cancer". C'est ce qu'ont décidé les Experts Européens lors de la réunion (28ème Adaptation au Progrès Technique) du 25 janvier 2001, confirmant ainsi la recommandation du groupe de travail de l'Union Européenne, chargé de la classification, de l'emballage et de l'étiquetage. Rappelons que le trichloréthylène était en catégorie 3 des cancérogènes, étiqueté R40 "Effet cancérogène suspecté-preuves insuffisantes".
Contamination au TCE
La municipalité de Shannon, municipalité de la province de Québec (Canada) réalise des analyses et remarque que la nappe phréatique est contaminée par du trichloréthylène (TCE), ce qui cause une augmentation des cancers dans cette région. Les gens de la ville ont décidé d'intenter un recours collectif contre le gouvernement du Canada car celui-ci connaissait le problème depuis 30 ans[7] .
Un cluster de cancer (leucémie et autres), impliquant des composés organiques volatiles dégagés par une entreprise de nettoyage à sec, dont du trichloréthylène, du 1,2-dichloroéthylène, du perchloroéthylène, du dichlorométhane et du chlorure de vinyle, a été découvert à Camp Lejeune, en Caroline du Nord [8].
Recherche
- 2007. Des chercheurs de l'Université de Washington ont développé un peuplier OGM capable de métaboliser et détruire le trichloréthylène souillant des sites industriels pollués. [réf. nécessaire]
Notes et références
- ↑ a , b , c , d , e , f , g , h et i TRICHLOROETHYLENE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ ESIS. Consulté le 1 février 2009
- ↑ IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 2A : Probablement cancérogènes pour l'homme » sur http://monographs.iarc.fr, 16 janvier 2009, CIRC. Consulté le 22 août 2009
- ↑ « Trichloréthylène » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- ↑ carcinogène : qui peut donner le cancer (synonymes : cancérigène, cancérogène)
- ↑ [1] Radio-Canada - Reportage: Cancers à Shannon
- ↑ Agency for Toxic Substances and Disease Registry (ATSDR), Survey of Childhood Cancers and Birth Defects at USMC Camp Lejeune (Full Report), juillet 2003.
Liens externes
- Le nouvel étiquetage du Trichloréthylène : la reclassification et ses conséquences, un article du site http://fr.prevent.be/
- Portail de la chimie
Catégories : Produit chimique toxique | Cancérogène chimique | Produit chimique dangereux pour l'environnement | Halogénure organique | Solvant | Composé du chlore
Wikimedia Foundation. 2010.


