- 76-22-2
-
Camphre
Camphre 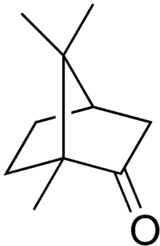
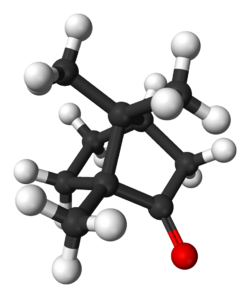
Général Nom IUPAC 1,7,7-triméthylbicyclo[2,2,1]heptan-2-one Synonymes 2-Bornanone
2-CamphanoneNo CAS No EINECS FEMA Apparence cristaux incolores ou blancs, d'odeur caractéristique.[1] Propriétés chimiques Formule brute C10H16O [Isomères] Masse molaire 152,2334 g∙mol-1
C 78,9 %, H 10,59 %, O 10,51 %,Propriétés physiques T° fusion 180 °C, la substance sublime à température ambiente.[1] T° ébullition 204 °C[1] Solubilité dans l'eau à 25 °C : 0.12 g/100 ml[1] Masse volumique 0.99 g/cm³[1] T° d’auto-inflammation 466 °C[1] Point d’éclair 66 °C (c.f.)[1] Limites d’explosivité dans l’air en volume % dans l'air : 0.6-3.5[1] Pression de vapeur saturante à 20 °C : 27 Pa[1] Précautions NFPA 704 SIMDUT[2] 
Unités du SI & CNTP, sauf indication contraire. Le camphre est un composé aromatique solide issu du camphrier, connu scientifiquement comme "Cinnamomum camphora". Le camphre, de formule C10H16O, est blanc, volatil, d'odeur vive. C'est une cétone à partir de laquelle on synthétise le bornéol et le camphène. Quasi insoluble dans l'eau, il est soluble dans les solvants organiques.
Le nom "camphre" vient du latin médiéval camfora, provenant de l'arabe al kafur (الكافور), du nom malais kapur Barus qui veut dire "craie de Barus". Les marchands malais qui vendaient le camphre aux négociants venus d'Inde et du Moyen-Orient l'appelaient kapur à cause de sa couleur blanche. Barus était le port sur la côte ouest de l'ile indonésienne de Sumatra où les marchands étrangers venaient acheter le camphre.
Il ne faut pas confondre le camphre de Bornéo contenant du Bornéol C10H18O et extrait de "Dryobalanops camphora" avec celui extrait de "Laurus camphora".
Le camphre est récupéré par distillation de morceaux de racines, de tiges ou d'écorces du camphrier. Les feuilles de certaines plantes, comme les matricaires, contiennent une forme de camphre non commercialisée. Une autre forme, constituée d'un mélange d'isomères, se trouve dans l'huile d'un chrysanthème asiatique, et est également synthétisée pour la plupart des utilisations commerciales.
Au Japon, on préparait le camphre en faisant passer de la vapeur d'eau sur des copeaux de camphrier (Laurus camphora); le camphre était alors entrainé par la vapeur et venait se condenser sur des chapiteaux de paille où on le recueillait. On obtenait ainsi le camphre brut, qui était exporté, et qu'il fallait encore purifier en le sublimant dans des ballons de verre après l'avoir mélangé à 3 à 5 % de chaux récemment éteinte. Les ballons étaient ensuite chauffés avec de grandes précautions, dans un bain de sable, tout en élevant progressivement la température jusqu'à 205°. Le camphre se sublimait alors et venait former, dans la partie supérieure du ballon un amas que l'on récupérait en brisant le verre.
Il existe aussi de nombreuses méthodes pour synthétiser le camphre. L'une d'entre elles a pour point de départ l'essence de thérébentine ou pinène C10H16. Berthelot synthétisa aussi le camphre par oxydation du bornéol C10H18O ou du camphène C10H16
Sommaire
Propriétés chimiques
Masse cristalline incolore, translucide, onctueuse au toucher, rayée par l'ongle, d'odeur vive, de saveur amère, aromatique. Sa densité est de 0,992 à 10°. Il se sublime à la température ordinaire (à l'air libre) à cause de sa tension de vapeur non négligeable. Pur, il fond à 179,75 °C et bout à 204 °C[réf. nécessaire].
Il est soluble dans 840 parties d'eau, insoluble dans la glycérine, soluble dans 0,65 parties d'alcool à 95°, très soluble dans l'éther, la benzine, l'acide acétique, les huiles et les essences. Sa solution alcoolique est dextrogyre et le degré varie avec la concentration et la provenance. Si le camphre extrait des laurinées dévie la lumière polarisée à droite, il existe un camphre levogyre extrait de l'huile essentielle de matricaire.
L'acide nitrique le transforme en acide camphorique C10H16O4.Le camphre brule à l'air avec une flamme fuligineuse.
Bien que le camphre puisse être utilisé dans la fabrication d'explosifs, il n'est pas explosif lui-même : comme tout produit combustible volatil ses vapeurs mélangées à l'air peuvent exploser.Utilisations
- Le camphre est utilisé dans la production du celluloïd, d'explosifs, ainsi qu'en médecine pour ses propriétés antiseptiques et légèrement anesthésiques. Cependant, le camphre est un poison lorsqu'il est ingéré en grandes quantités. Le camphre est un anaphrodisiaque[1]
- Le camphre a été utilisé pour lutter contre l'épidémie de choléra-morbus en 1831-1832 puis contre la grippe asiatique en 1957-1958.
- Sa propriété de repousser l'eau le faisait utiliser dans les années 1950 comme « moteur » pour de petits jouets flottants : ces jouets en plastique très léger étaient posés sur une petite plaque de celluloïd dans laquelle on sertissait deux ou trois cylindres de camphre d'un peu plus d'un millimètre : le jouet se déplaçait lentement par exemple dans une cuvette d'eau. Le jouet était fourni avec une trentaine de cartouches.
- De plus, le camphre est utilisé dans le tir sportif, notamment au pistolet, pour noircir les organes de visée en le faisant brûler car il dégage une fumée noire.
Anecdotes
- Dans La machine à explorer le temps de H. G. Wells, c'est en enflammant du camphre resté intact dans le flacon scellé d'un musée que le voyageur du temps met en fuite les Morlocks.
Références
- ↑ a , b , c , d , e , f , g , h et i CAMPHRE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ « Camphre synthétique » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Portail de la chimie
Catégories : Composé cyclique | Terpènes et terpénoïdes | Cétone | Arôme | Goût frais
Wikimedia Foundation. 2010.