- 53-84-9
-
Nicotinamide adénine dinucléotide
 Pour les articles homonymes, voir NAD.
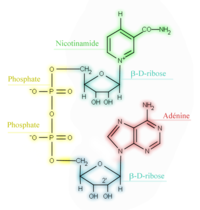
Pour les articles homonymes, voir NAD.Nicotinamide adénine dinucléotide Figure 1 : La forme oxydée du nicotinamide adénine dinucléotide (NAD+) Général Synonymes NAD+
Coenzyme INo CAS No EINECS DrugBank SMILES InChI Apparence solide Propriétés chimiques Formule brute C21H27N7O14P2 Masse molaire 663,4251 g∙mol-1
C 38,02 %, H 4,1 %, N 14,78 %, O 33,76 %, P 9,34 %,Écotoxicologie DL50 4333mg/kg (souris, i.p.)[1] Unités du SI & CNTP, sauf indication contraire. Le Nicotinamide adénine dinucléotide abrégé en NAD est une coenzyme d'oxydoréduction présent dans toutes les cellules vivantes. Le composé est un dinucléotide, puisqu'il est composé de deux nucléotides liés par leurs groupes phosphate. Un des nucléotides contient une adénine tandis que l'autre contient un nicotinamide. Dans le métabolisme, le NAD+ est impliqué dans les réactions redox en transportant des électrons. Cette coenzyme est présente sous deux formes dans la cellule. NAD+ est un agent d'oxydation et NADH est un agent de réduction. Le transfert d'électron est la principale fonction du NADH.
Sommaire
Structure
Le NAD est dérivé de la vitamine B3 (ou vitamine PP) : la nicotinamide.
La figure 1 présente la structure du NAD+ (forme oxydée). Ce coenzyme n'est pas fixé sur l'apoenzyme, c'est un cosubstrat.
Mode d'action
Le coenzyme fixe réversiblement un ion H+ et un électron sur le noyau nicotinamide (figure 2) en présence d'une enzyme de la classe des oxydoréductases.
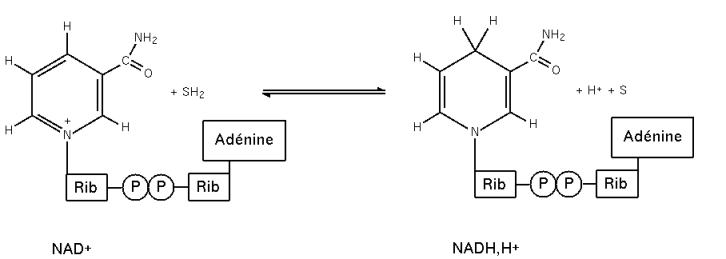 Figure 2 : réaction d'oxydo-réduction du NAD.
Figure 2 : réaction d'oxydo-réduction du NAD.Le couple oxydant/réducteur est le suivant :
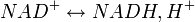
Intérêt en biochimie analytique
Il réside dans une propriété physique particulière : le NAD+ possède un maximum d'absorption en ultraviolet à 260 nm ; la forme réduite (NADH) quant à elle possède deux maxima d'absorption en UV, un premier à 260 nm et un second à 340 nm. En suivant l'absorbance à 340 nm, on pourra suivre l'évolution de la réaction enzymatique, une augmentation d'absorbance indiquant une formation de NADH (la réaction va dans le sens de la réduction du substrat) tandis qu'une diminution d'absorbance indique la consommation de NADH, donc une formation de NAD+ (la réaction va dans le sens de l'oxydation du substrat). La courbe
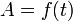 correspond à la cinétique d'apparition ou de disparition du NADH. A partir de cette courbe, il est possible de calculer la vitesse initiale de la réaction (voir Équation de Michaelis Menten).
correspond à la cinétique d'apparition ou de disparition du NADH. A partir de cette courbe, il est possible de calculer la vitesse initiale de la réaction (voir Équation de Michaelis Menten).Le coefficient d'extinction molaire de la forme réduite (NADH) à 340 nm = 6,22 103 mol-1.L.cm-1
Rôle dans le métabolisme
Le NAD est une coenzyme qui est présente dans toutes les cellules et qui aide les enzymes à tranférer les électrons pendant les réactions d'oxydo-réductions du métabolisme de formation de l'ATP.
Notes et références
- ↑ (en) « Nadide » sur ChemIDplus, consulté le 16 août 2009
- Portail de la biochimie
Catégories : Composé du phosphore | Coenzyme
Wikimedia Foundation. 2010.