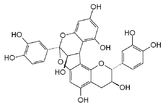
- Procyanidine
-
Les procyanidines ou procyanidols sont des tanins condensés formés par des unités flavaniques de type catéchol et épicatéchol[1]. Par ébullition en milieu acide, ils libèrent un pigment rouge, le cyanidol (un anthocyanidol).
Ce sont les proanthocyanidols les plus abondants chez les plantes, suivis par les prodelphinidols.
Sommaire
Structures
Les dimères les plus communs sont[2].
- Procyanidols de type B-1, B-2, B-3 et B-4
Ce sont des dimères constitués à partir des deux unités (+)-catéchol et (-)-épicatéchol, liées en C-4 → C-8.
- Procyanidols de type B-5, B-6, B-7 et B-8
Ce sont des dimères constitués aussi à partir des deux unités (+)-catéchol et (-)-épicatéchol mais avec une liaison en C-4 → C-6.
Structures chimiques des proanthocyanidols dimériques de type B, d'après Perret[2] (2001) 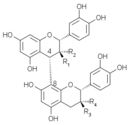
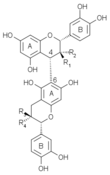
Dimères Noms R1 R2 R3 R4 B1 épicatéchol-(4β→8)-catéchol H OH OH H B2 épicatéchol-(4β→8)-épicatéchol H OH H OH B3 catéchol-(4α→8)-catéchol OH H OH H B4 catéchol-(4α→8)-épicatéchol OH H H OH B5 épicatéchol-(4β→6)-épicatéchol H OH H OH B6 catéchol-(4α→6)-catéchol OH H OH H B7 épicatéchol-(4β→6)-catéchol H OH OH H B8 catéchol-(4α→6)-épicatéchol OH H H OH Il existe aussi des O- et C-glucosides de procyanidols, par exemple chez la rhubarbe et le théier.
- Les procyanidols de type A sont des dimères ayant une liaison interflavanique double :
- 1) liaison C-4 → C-8 et
- 2) liaison éther C-2 → O → C-7.
- Les oligomères et polymères construits sur les unités (épi)catéchols et libérant du cyanidol sont très communs et abondants. Pour certains auteurs[3], le terme de « procyanidines oligomériques ou polymériques » en est venu à désigner la classe entière des proanthocyanidols ou tanins condensés[4].
Propriétés
Comme tous les proanthocyanidols, les procyanidols sont réputés pour leur forts pouvoirs antioxydants.
On a longtemps cru que l'effet bénéfique du vin était dû au resvératrol, il semble plutôt que ce soient dû aux procyanidines. C'est du moins ce que tendent à démontrer les recherches du professeur Roger Corder du Queen Mary’s School of Medicine de Londres.
Les procyanidines alimentaires joueraient un rôle-clé dans la modification du fonctionnement vasculaire. Les vins produits dans les régions où la population vit plus longtemps que la moyenne contiennent des taux de procyanidines beaucoup plus élevées que les vins d'autres régions[5].
Dans le raisin, ils proviennent des pépins. On en trouve surtout dans les vins rouges jeunes, tanniques, provenant de vieilles vignes, en altitude, aux petits rendements, aux petites baies et à macération longue. Certains cépages en contiennent plus que d'autres. Les cépages tanniques justement : tannat, malbec, mondeuse, sagrantino et cabernet sauvignon.
La filtration, le collage, la surmaturité et le vieillissement du vin réduiraient la quantité de procyanidines[5].
Notes et références
- Bruneton, J., Pharmacognosie - Phytochimie, plantes médicinales, 4e éd., revue et augmentée, Paris, Tec & Doc - Éditions médicales internationales, 2009, 1288 p. (ISBN 978-2-7430-1188-8)
- Camille Perret, Analyse de tannins inhibiteurs de la stilbène oxydase produite par Botrytis cinera, Thèse de l'université de Neuchâtel, faculté des sciences, 2001
- comme Roger Corder et ses collaborateurs [1], mais nous préférons la terminologie plus précise de Jean Bruneton
- Red wine procyanidins and vascular health
- (fr)Présentation du livre : Boire mieux pour vivre vieux, 5 juin 2010 — Marc André Gagnon sur vinquebec.com. Consulté le 25 juin 2010. Boire mieux pour vivre vieux
Annexes
Bibliographie
- Roger Corder, Boire mieux pour vivre vieux, Thierry Souccar Éditions, 2009 ( vinquebec.com Résumé du livre)
Liens externes
- (en) Transcription du Podcast avec le docteur Roger Corder, magazine Nature
- (en) Roger Corder, « Oenology: Red wine procyanidins and vascular health », Nature, 30 novembre 2006.
- (en) Roger Corder, [PDF] « Red wine procyanidins and vascular health », Nature
- (en) Fine AM, « Oligomeric proanthocyanidin complexes: history, structure, and phytopharmaceutical applications », dans Altern Med Rev, vol. 5, no 2, avril 2000, p. 144–51 [texte intégral, lien PMID]
- Portail de la vigne et du vin
- Portail de la chimie
Wikimedia Foundation. 2010.