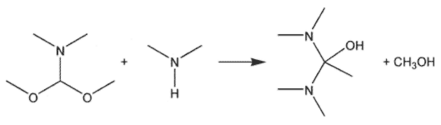Tétrakis(diméthylamino)éthylène
- Tétrakis(diméthylamino)éthylène
-
| Tétrakis(diméthylamino)éthylène |
 |
| Général |
| Nom IUPAC |
N1,N1,N1',N1',N2,N2,N2',N2'-octaméthyléthène-1,1,2,2-tétramine |
| Synonymes |
octaméthyléthylènetétramine
TDAE
TMAE |
| No CAS |
996-70-3 |
| No EINECS |
213-638-1 |
| PubChem |
70455
24885226 |
| SMILES |
|
| InChI |
InChI : Vue 3D
InChI=1/C10H24N4/c1-11(2)9(12(3)4)10(13(5)6)14(7)8/h1-8H3
|
| Apparence |
liquide légèrement jaune d'odeur désagréable |
| Propriétés chimiques |
| Formule brute |
C10H24N4 [Isomères]
|
| Masse molaire[1] |
200,3244 ± 0,0105 g·mol-1
C 59,96 %, H 12,08 %, N 27,97 %,
|
| Propriétés physiques |
| T° ébullition |
59 °C sous 0,9 mmHg[2] |
| Masse volumique |
0,861 g·cm-3 à 25 °C[2] |
| Point d’éclair |
53 °C[2] |
| Propriétés optiques |
| Indice de réfraction |
 1,48[2] 1,48[2] |
| Précautions |
|
Directive 67/548/EEC
|

Xi
|

C
|
|
Symboles :
Xi : Irritant
C : Corrosif
Phrases R :
R10 : Inflammable.
R34 : Provoque des brûlures.
Phrases S :
S26 : En cas de contact avec les yeux, laver immédiatement et abondamment avec de l’eau et consulter un spécialiste.
S45 : En cas d’accident ou de malaise, consulter immédiatement un médecin (si possible, lui montrer l’étiquette).
S36/37/39 : Porter un vêtement de protection approprié, des gants et un appareil de protection des yeux/du visage.
|
| Phrases R : 10, 34, |
| Phrases S : 26, 36/37/39, 45, |
|
Transport
|
Numéro ONU :
2734 : AMINES LIQUIDES, CORROSIVES, INFLAMMABLES, N.S.A.; ou POLYAMINES LIQUIDES, CORROSIVES, INFLAMMABLES, N.S.A.
Classe :
8
Étiquette :
 8
8 : Matières corrosives
Emballage :
Groupe d'emballage II : matières moyennement dangereuses;
|
|
Unités du SI & CNTP, sauf indication contraire.
|
Le tétrakis(diméthylamino)éthylène fait partie des énamines et a pour formule semi-développée [(CH3)2N]2C=C[N(CH3)2]2.
Synthèse
La synthèse du tétrakis(diméthylamino)éthylène a été réalisée pour la première fois en 1950[3]. Cependant la réaction de la (1,1-diméthoxyméthyl)diméthylamine avec la diméthylamine[4] est plus pratique :
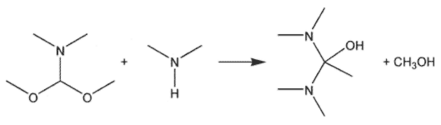
Le milieu réactionnel est distillé ce qui, par élimination du méthanol, conduit au tétrakis(diméthylamino)éthylène :
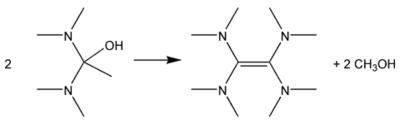
Usage
Le tétrakis(diméthylamino)éthylène est un réducteur qui réagit avec l'oxygène de l'air. Il sert habituellement de réducteur en chimie organique comme par exemple pour convertir des α-bromocétones en 1,4-dicétones[5].
Il forme aussi un sel à transfert de charge avec le fullerène C60 qui a la très rare propriété d'être un aimant purement organique en dessous de 16,1 K[6].
La réaction du tétrakis(diméthylamino)éthylène avec l'oxygène de l'air est chimioluminescente dans le bleu-vert. Elle permet ainsi de faire des effets spectaculaires comme « les mains lumineuses[7] ».
Notes et références
- ↑ Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- ↑ a, b, c et d fiche Sigma Aldrich et les références dessus
- ↑ R. L. Pruett ; J. T. Barr ; K. E. Rapp ; C. T. Bahner ; J. D. Gibson ; R. H. Lafferty ; J. Am. Chem. Soc., 1950, vol. 72, p. 3646.
- ↑ H. Eilingsfeld ; M. Seefelder ; H. Weidinger ; Chem. Ber. ; 1963, vol. 96, p. 2671.
- ↑ Tetrahedron Lett., 2006, vol. 47, p.5565.
- ↑ P.M. Allemand et al., Science, 1991, vol. 253, p. 301.
- ↑ les mains lumineuses expliquées sur le site de scienceamusante.
Wikimedia Foundation.
2010.
Contenu soumis à la licence CC-BY-SA. Source : Article Tétrakis(diméthylamino)éthylène de Wikipédia en français (auteurs)
Regardez d'autres dictionnaires:
996-70-3 — Tétrakis(diméthylamino)éthylène Tétrakis(diméthylamino)éthylène Général Nom IUPAC N1,N1,N1 ,N1 … Wikipédia en Français
C10H24N4 — Tétrakis(diméthylamino)éthylène Tétrakis(diméthylamino)éthylène Général Nom IUPAC N1,N1,N1 ,N1 … Wikipédia en Français
TDAE — Tétrakis(diméthylamino)éthylène Tétrakis(diméthylamino)éthylène Général Nom IUPAC N1,N1,N1 ,N1 ,N … Wikipédia en Français
TMAE — Tétrakis(diméthylamino)éthylène Tétrakis(diméthylamino)éthylène Général Nom IUPAC N1,N1,N1 ,N1 ,N … Wikipédia en Français
Endohedral hydrogen fullerene — or H2@C60 is an endohedral fullerene containing molecular hydrogen. This chemical compound has a potential application in molecular electronics and was synthesized in 2005 at Kyoto University by the group of Koichi Komatsu [ Synthesis, Structure … Wikipedia
One-electron reduction — A one electron reduction in organic chemistry involves the transfer of an electron from a metal to an organic substrate. It serves to differentiate between true organic reductions and other reductions such as hydride transfer reactions that… … Wikipedia
Buckminsterfullerène — « C60 » redirige ici. Pour le paquebot, voir Himalaya (paquebot). Buckminsterfullerène … Wikipédia en Français
Danishefsky Taxol total synthesis — overview from raw material perspective The Danishefsky Taxol total synthesis in organic chemistry is an important third Taxol synthesis published by the group of Samuel Danishefsky in 1996 [1] two years after the first two efforts … Wikipedia

 1,48[2]
1,48[2]